
Wetenschap
Verbinding die hydroxide -ionen vormt in oplossing?
Hier zijn enkele voorbeelden:
* metaalhydroxiden: Dit zijn ionische verbindingen die een metaalkation en het hydroxide-anion (OH-) bevatten. Voorbeelden zijn natriumhydroxide (NaOH), kaliumhydroxide (KOH) en calciumhydroxide (CA (OH) 2).
* Sommige niet-metalen oxiden: Bepaalde niet-metale oxiden reageren met water om zuren te vormen, die vervolgens hydroxide-ionen afgeven. Zwaveldioxide (SO2) reageert bijvoorbeeld met water om zwavelzuur (H2SO3) te vormen, die vervolgens hydroxide -ionen vrijgeeft.
* ammoniumhydroxide (NH4OH): Hoewel het geen echte hydroxide is, is ammoniumhydroxide een zwakke basis die ammoniumionen (NH4+) en hydroxide-ionen (OH-) in oplossing vormt.
Het vermogen van een verbinding om hydroxide -ionen in oplossing te vormen, maakt het een basis. Bases worden gekenmerkt door hun gladde gevoel, bittere smaak en het vermogen om zuren te neutraliseren.
 Machine-learning aardbevingsvoorspelling in laboratorium veelbelovend
Machine-learning aardbevingsvoorspelling in laboratorium veelbelovend Waarom stopt uw filter aarde in het zwembad?
Waarom stopt uw filter aarde in het zwembad?  Wat is spanning in planten?
Wat is spanning in planten?  Oranje is het nieuwe groen:hoe sinaasappelschillen een Costa Ricaans bos nieuw leven inblazen
Oranje is het nieuwe groen:hoe sinaasappelschillen een Costa Ricaans bos nieuw leven inblazen Reactie op coronavirus vertraagt nauwelijks stijgende kooldioxide
Reactie op coronavirus vertraagt nauwelijks stijgende kooldioxide
Hoofdlijnen
- Waarom eten zeevogels plastic? Het antwoord stinkt
- Hoe hybride plantenrassen de uitdagingen van voedselzekerheid en klimaatverandering kunnen aanpakken
- Wat zijn homologieën en waarom ze belangrijk zijn in classificatie?
- Welk gewricht zal zich uiteindelijk ontwikkelen tot een synostose?
- NOAA bevestigt vierde wereldwijde koraalverblekingsgebeurtenis
- Welke soorten organismen doen stikstoffixatie?
- Hoe zou je suikerwater classificeren?
- Hoe komt stikstof uit levende organismen terug in de lucht?
- Genezing van verbrande poten met vissenhuid
- Een nieuwe manier om verspild methaan te benutten
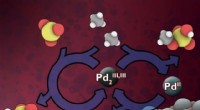
- Multifunctionele droom keramische matrixcomposieten zijn geboren

- Video:De toevallige ontdekking van LSD

- Onderzoekers die een instrument ontwerpen om uranium te identificeren, atomen tegelijk

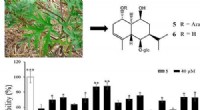
- Ambrosia-verbindingen kunnen zenuwcellen beschermen tegen Alzheimer
 Nieuwe studies zijn bedoeld om sociaalwetenschappelijke methoden in natuurbehoudonderzoek te stimuleren
Nieuwe studies zijn bedoeld om sociaalwetenschappelijke methoden in natuurbehoudonderzoek te stimuleren Wat zijn niet-metaal elementen?
Wat zijn niet-metaal elementen?  Wat gebeurt er in een Brønsted-Lowry zuur-base reactie?
Wat gebeurt er in een Brønsted-Lowry zuur-base reactie?  Ethiopische luchtvaartmaatschappij verdedigt de trainingsnormen voor piloten
Ethiopische luchtvaartmaatschappij verdedigt de trainingsnormen voor piloten Waterstof in plaats van elektrificatie? Potenties en risico's voor klimaatdoelen
Waterstof in plaats van elektrificatie? Potenties en risico's voor klimaatdoelen Wat zijn de rollen van organismen?
Wat zijn de rollen van organismen?  Hoeveel 2 gram keer 17 is gelijk aan kilo's?
Hoeveel 2 gram keer 17 is gelijk aan kilo's?  Vraag en antwoord:Expert bespreekt hoe belangrijk het is om verstandig te worden met verkeerde informatie, complottheorieën
Vraag en antwoord:Expert bespreekt hoe belangrijk het is om verstandig te worden met verkeerde informatie, complottheorieën
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

