
Wetenschap
Hoe wordt oxide -ion gevormd?
* elektronische configuratie van Oxygen: Een neutraal zuurstofatoom heeft 8 elektronen, met de elektronische configuratie 1S
* Verlangen naar stabiliteit: Zuurstof wil, zoals de meeste elementen, een stabiele elektronenconfiguratie bereiken. Dit betekent een volledige buitenste schaal van 8 elektronen.
* Elektronen verkrijgen: Om dit te bereiken, kan zuurstof twee elektronen krijgen en een anion worden (negatief geladen ion).
* Vorming van oxide -ionen: Wanneer zuurstof deze twee elektronen wint, vult het zijn buitenste schaal en wordt het oxide-ion (o
2-
).
Hier is een vereenvoudigde visual:
`` `
O + 2e- → o²⁻
`` `
Sleutelpunten:
* De vorming van oxide -ionen is een veel voorkomend proces in de chemie, met name bij de vorming van ionische verbindingen.
* Het oxide-ion draagt een 2- lading vanwege het verkrijgen van twee negatief geladen elektronen.
* Dit proces is een voorbeeld van elektronenaffiniteit , waarbij een atoom elektronen krijgt om een stabielere elektronische configuratie te bereiken.
 Welk experiment overtuigde Ernest Rutherford dat het atoom een kleine positiviteitskleur heeft?
Welk experiment overtuigde Ernest Rutherford dat het atoom een kleine positiviteitskleur heeft?  Wanneer ammoniumbromide en natriumhydroxide gemengd zijn, wat is de chemische vergelijking?
Wanneer ammoniumbromide en natriumhydroxide gemengd zijn, wat is de chemische vergelijking?  Hoe verschillen de massa's van atomen die worden geproduceerd als resultaatfusiereactie van die nucleaire splijtingsreactie?
Hoe verschillen de massa's van atomen die worden geproduceerd als resultaatfusiereactie van die nucleaire splijtingsreactie?  Waarom wordt HCl gebruikt bij de titratie van mohrzout en kaliumdichromaat?
Waarom wordt HCl gebruikt bij de titratie van mohrzout en kaliumdichromaat?  Een mengsel van 0,220 mol CO 0,350 H2 en 0,640 Hij heeft een totale druk van 2,95 Atm, wat is de H2?
Een mengsel van 0,220 mol CO 0,350 H2 en 0,640 Hij heeft een totale druk van 2,95 Atm, wat is de H2?
 Australië lanceert droogteplan van miljard dollar
Australië lanceert droogteplan van miljard dollar Verhoogt of neemt de diversiteit af na een brand op grasland?
Verhoogt of neemt de diversiteit af na een brand op grasland?  Het verwijderen van plastic zwerfvuil op zee is kostbaar voor kleine eilandstaten
Het verwijderen van plastic zwerfvuil op zee is kostbaar voor kleine eilandstaten Beukenboom groeit als klimaatveranderingen, en dat is slecht voor de bossen
Beukenboom groeit als klimaatveranderingen, en dat is slecht voor de bossen Bos bereikt hun grootste ecologische complexiteit wanneer?
Bos bereikt hun grootste ecologische complexiteit wanneer?
Hoofdlijnen
- Microscopische plooien die zich uitstrekken van het apicale oppervlak van bepaalde epithelia om het gebied voor absorptie en secretie te vergroten?
- Roadkill-pieken van fazanten in de herfst en late winter
- Wat is het verschil tussen krijgskunst en wetenschap?
- Wat is de definitie voor verdamping in wetenschapstermen?
- Diagram om de relatie tussen cellen en volledig organisme te tonen?
- Nieuwe AI-tool legt vast hoe eiwitten zich in context gedragen
- Wat is een basisverschil tussen protisten en schimmels?
- Wat gebeurt er in kankercellen tijdens deling?
- Is een regenboog biotisch of abiotisch?
- Wetenschappers bedenken diervrije testen van dodelijke neurotoxines

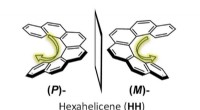
- Hoop op ontwikkeling van materialen voor 3D-displays en medische toepassingen
- Gebruikmakend van de kracht van CRISPR-Cas9 om antibiotica te wekken uit hun stille genclusters
- Wetenschappers ontwerpen veelbelovende nieuwe kathode voor op natrium gebaseerde batterijen

- Kleurcodering moleculaire spiegelbeelden
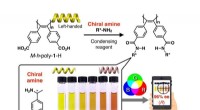
 Welke binding is eigenlijk meer een aantrekking en vindt plaats tussen watermoleculen?
Welke binding is eigenlijk meer een aantrekking en vindt plaats tussen watermoleculen?  Ionotronische technologie waarvoor geen vloeibare elektrolyten nodig zijn
Ionotronische technologie waarvoor geen vloeibare elektrolyten nodig zijn Welke cel staat bekend als de krachtpatsercel?
Welke cel staat bekend als de krachtpatsercel?  Wat hoort thuis in de lege ruimte van de chemische vergelijking voor het verbranden van fossiele brandstoffen hieronder?
Wat hoort thuis in de lege ruimte van de chemische vergelijking voor het verbranden van fossiele brandstoffen hieronder?  Waarom zouden tien wetenschappers allemaal hetzelfde experiment uitvoeren?
Waarom zouden tien wetenschappers allemaal hetzelfde experiment uitvoeren?  Europa's oudste meer sporen 1,36 miljoen jaar klimaat
Europa's oudste meer sporen 1,36 miljoen jaar klimaat Een algoritme om invloeden van buitenaf op de media te detecteren
Een algoritme om invloeden van buitenaf op de media te detecteren Welke energie gebruikt een waterkoker om water te verwarmen?
Welke energie gebruikt een waterkoker om water te verwarmen?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

