
Wetenschap
Als 6.0 g ijzer met chloor reageert, wat is het maximale aantal mol mengelmoes-II-chloride dat kan worden geproduceerd?
Hier is hoe dit probleem op te lossen:
1. Schrijf de gebalanceerde chemische vergelijking:
Fe (s) + cl₂ (g) → fecl₂ (s)
2. Bereken de mol ijzer:
* Molaire massa van ijzer (Fe) =55.845 g/mol
* Mol Fe =(6,0 g) / (55,845 g / mol) =0,107 mol
3. Bepaal de molverhouding:
* Uit de evenwichtige vergelijking reageert 1 mol Fe om 1 mol Fecl₂ te produceren.
4. Bereken het maximale mol ijzer-II chloride (Fecl₂):
* Aangezien de molverhouding 1:1 is, is de maximale mol fecl₂ geproduceerd gelijk aan de mol Fe:0,107 mol Fecl₂
Antwoord: Het maximale aantal mol ijzer-II-chloride (FECL₂) dat kan worden geproduceerd, is 0,107 mol .
 Wat is de pH-waarde van aardolie?
Wat is de pH-waarde van aardolie?  Wat zijn de reactanten voor koolstofdioxide met zout en water?
Wat zijn de reactanten voor koolstofdioxide met zout en water?  Wat zijn de belangrijkste ingrediënten van zoutwater?
Wat zijn de belangrijkste ingrediënten van zoutwater?  Materialen volgen de 'Regel van Vier', maar wetenschappers weten nog niet waarom
Materialen volgen de 'Regel van Vier', maar wetenschappers weten nog niet waarom  Controle over de Amerikaanse Senaat:wat vertelt de geschiedenis ons over de mate waarin dit de beleidsvorming op wetgevingsgebied beïnvloedt?
Controle over de Amerikaanse Senaat:wat vertelt de geschiedenis ons over de mate waarin dit de beleidsvorming op wetgevingsgebied beïnvloedt?
 Welke dieren kauwen boomtakken af?
Welke dieren kauwen boomtakken af?  Het effect van alcohol op planten
Het effect van alcohol op planten Wat is een ecoculturele identiteit?
Wat is een ecoculturele identiteit? Kinderen leren over klimaatverandering, hoop inspireren en actie ondernemen om de toekomst te veranderen
Kinderen leren over klimaatverandering, hoop inspireren en actie ondernemen om de toekomst te veranderen Bergen aan gegevens:een ongekend klimaatobservatorium om de toekomst van water te begrijpen
Bergen aan gegevens:een ongekend klimaatobservatorium om de toekomst van water te begrijpen
Hoofdlijnen
- Wat wordt overgebracht van organisme naar in een voedselketen?
- Nieuw soort cognitieve robot... een puppy?
- Welke zaadloze plant heeft geen transportweefsel?
- Uit een fossiel gevonden in Duitsland blijkt dat een familielid van zeesterren 150 miljoen jaar geleden betrokken was bij klonale fragmentatie
- In ons lichaam zijn teams van microben aan het werk. Onderzoekers hebben ontdekt waar ze mee bezig zijn.
- Wat veroorzaakt apicale dominantie?
- Hoe overleven blinde grotvissen hun zuurstofarme omgeving?
- Een nieuw quarantaineschema zou het risico op herintroductie van hondsdolheid in de EU na de Russische invasie kunnen verminderen, zo blijkt uit onderzoek
- Wat is het forumla voor fotosynthese?
- Onderzoekers ontwikkelen taaie, zelfherstellend rubber

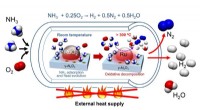
- Ontdekking van een eenvoudig proces voor H2-productie met ammoniak als drager
- Nieuwe toepassingen vinden voor afvalbanden

- Driedimensionale Mn-gedoteerde nanosheets als efficiënte elektrokatalysatoren voor het splitsen van alkalisch water

- Video:Petrichor, de geur van regen

 Wat is de molaire massa van B10H14?
Wat is de molaire massa van B10H14?  Leg nucleaire fusie uit en hoe het de zon voedt?
Leg nucleaire fusie uit en hoe het de zon voedt?  Wrijving gevonden waar er geen zou moeten zijn - in superfluïde nabij het absolute nulpunt
Wrijving gevonden waar er geen zou moeten zijn - in superfluïde nabij het absolute nulpunt Onderzoekers demonstreren nieuwe concepten voor warmtemanagement
Onderzoekers demonstreren nieuwe concepten voor warmtemanagement Een riskante weg om de klimaatdoelstellingen voor Stockholm te halen
Een riskante weg om de klimaatdoelstellingen voor Stockholm te halen  Hoe wordt grafiet geëxtraheerd?
Hoe wordt grafiet geëxtraheerd?  Hoe worden rotsen in de zee genoemd?
Hoe worden rotsen in de zee genoemd?  Wat gebeurt er met een dierlijke cel in een hypotone oplossing?
Wat gebeurt er met een dierlijke cel in een hypotone oplossing?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

