
Wetenschap
Wat is de geometrie van elektronenparen voor ammoniumion?
De geometrie van de elektronenparen van het ammoniumion (NH₄⁺) is tetraëdral .
Dit is waarom:
* centraal atoom: Stikstof (n)
* Aantal valentie -elektronen op N: 5
* Aantal obligaties aan n: 4 (één voor elk waterstofatoom)
* Aantal eenzame paren op n: 0
Het stikstofatoom heeft 4 elektronendomeinen, die elk een binding vertegenwoordigen aan een waterstofatoom. Volgens de VSEPR -theorie resulteren 4 elektronendomeinen in een geometrie van tetraëdrische elektronenparen.
 Communicatie tussen rotors in moleculaire motor voor het eerst waargenomen
Communicatie tussen rotors in moleculaire motor voor het eerst waargenomen  Sugar Faster
Sugar Faster Is natrium een pure stof of mengsel?
Is natrium een pure stof of mengsel?  Wat is het proces waarbij moleculen van een gebied met een hoge concentratie naar een gebied met een lage concentratie bewegen zonder de aanwezigheid van een membraan?
Wat is het proces waarbij moleculen van een gebied met een hoge concentratie naar een gebied met een lage concentratie bewegen zonder de aanwezigheid van een membraan?  Wat is de dichtheid van 1 molair natriumhydroxide in gram per milliliter?
Wat is de dichtheid van 1 molair natriumhydroxide in gram per milliliter?
 Heeft Catfish Lay Eggs?
Heeft Catfish Lay Eggs?  Hoe hydrologie werkt
Hoe hydrologie werkt  Zal Parijs slagen? Onderzoek beoordeelt of regeringen toezeggingen zullen waarmaken
Zal Parijs slagen? Onderzoek beoordeelt of regeringen toezeggingen zullen waarmaken In droge Antarctische valleien, vroege tekenen van door klimaatverandering veroorzaakte verschuivingen in de bodem
In droge Antarctische valleien, vroege tekenen van door klimaatverandering veroorzaakte verschuivingen in de bodem Onderzoek voorspelt een milieuramp als gevolg van de verwijdering van menstruatieproducten in India
Onderzoek voorspelt een milieuramp als gevolg van de verwijdering van menstruatieproducten in India
Hoofdlijnen
- Analyse van miljarden Twitter-woorden laat zien hoe Amerikaans Engels zich ontwikkelt
- Welke stoffen hebben planten nodig zodat ze aminozuren kunnen maken?
- Hoe vogelgriep werkt
- Hoe ondersteunt biogeografie de evolutietheorie?
- Wat is wetenschappelijke hypothesen?
- Waarom komt gisting voor in schimmels?
- Lasers en een aangepaste microscoop tonen het gensplitsingsproces in realtime
- De ongelooflijke reis van de eerste Afrikaanse schildpad die in Europa aankwam
- Hoe DNA wordt vernietigd door virus?
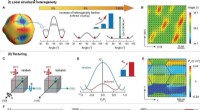
- Ultrahoge piëzo-elektrische prestaties aangetoond in keramische materialen
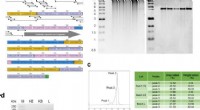
- Recombinant collageenpolypeptide als een veelzijdig biomateriaal voor bottransplantaten
- Nieuwe theorie belooft een nieuwe vorm te geven aan hoe we denken over polymeersuperstructuren

- Onderzoekers ontwikkelen 's werelds eerste aerogels gemaakt van schrootbanden

- Onderzoek naar de effecten van vocht en drogen op cement

 Studie onderzoekt de chemische stof GenX in water:is het anders dan andere PFAS?
Studie onderzoekt de chemische stof GenX in water:is het anders dan andere PFAS? Southwest vertraagt hervatting Boeing 737 MAX-vluchten
Southwest vertraagt hervatting Boeing 737 MAX-vluchten Rockoons maakt het lanceren van satellieten in de ruimte binnenkort mogelijk toegankelijker
Rockoons maakt het lanceren van satellieten in de ruimte binnenkort mogelijk toegankelijker Lipide nanodeeltjes die mRNA aan T-cellen afleveren, zijn veelbelovend tegen auto-immuunziekten
Lipide nanodeeltjes die mRNA aan T-cellen afleveren, zijn veelbelovend tegen auto-immuunziekten  Welke temperatuur verandert vloeistof tot een vaste stof?
Welke temperatuur verandert vloeistof tot een vaste stof?  Wat is het voordeel van het gebruik van wetenschappelijke notatie om getallen uit te drukken die erg klein en groot zijn?
Wat is het voordeel van het gebruik van wetenschappelijke notatie om getallen uit te drukken die erg klein en groot zijn?  Minderheidsgroepen zijn ondervertegenwoordigd in opiniepeilingen
Minderheidsgroepen zijn ondervertegenwoordigd in opiniepeilingen Soorten distillatie
Soorten distillatie
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

