
Wetenschap
Wat is de dichtheid van 1 molair natriumhydroxide in gram per milliliter?
1. Begrijp molariteit
* Molariteit (M) is een concentratie -eenheid die het aantal mol opgeloste oplossing vertegenwoordigt in 1 liter oplossing.
* In dit geval betekent een 1 M NaOH -oplossing dat er 1 mol NaOH is opgelost in 1 liter oplossing.
2. Bereken de massa van NaOH
* De molaire massa van NaOH is ongeveer 40 g/mol (23 g/mol voor Na + 16 g/mol voor o + 1 g/mol voor h).
* Omdat we 1 mol NaOH hebben, is de massa NaOH in 1 liter oplossing 40 gram.
3. Overweeg het volume en de dichtheid
* Dichtheid is massa per volume -eenheid (meestal gram per milliliter of g/ml).
* We kennen de massa NaOH (40 gram) en het volume van de oplossing (1 liter of 1000 ml).
4. Bereken de dichtheid
* Dichtheid =massa / volume
* Dichtheid =40 gram / 1000 ml
* Dichtheid =0,04 g/ml
Belangrijke opmerking: Deze berekening veronderstelt dat het volume van de oplossing ongeveer gelijk is aan het volume van het water. In werkelijkheid veroorzaakt het oplossen van NaOH in water een lichte toename van het volume. Daarom zal de werkelijke dichtheid van een 1 M NaOH -oplossing iets lager zijn dan 0,04 g/ml.
om een meer accurate dichtheid te krijgen:
* U zou experimenteel de dichtheid van de oplossing moeten meten met behulp van een dichtheidsmeter of een precieze weegmethode.
* U kunt dichtheidstabellen of online bronnen vinden die dichtheden bieden van verschillende concentraties NaOH -oplossingen.
Hoofdlijnen
- Hoe een nucleaire aanval op Noord-Korea zou bijdragen aan de mondiale kankerepidemie
- Hoe antibioticagebruik bij dieren bijdraagt aan antibioticaresistentie
- Waarom hebben zoveel van onze huisdieren overgewicht?
- Onderzoekers onthullen hoe het gehoor is geëvolueerd
- Wat zou er gebeuren als een celmembraan moeilijk zou worden?
- Activisten willen brug over snelweg bouwen om wilde dieren veilig over te steken
- Waar gaat deze altijd deel uit van de wetenschappelijke methode?
- Hoe wordt opgeslagen voedsel in een cel genaamd?
- Wat is algemene test voor eiwitten?
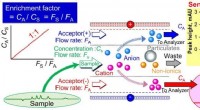
- Verbetering van de gevoeligheid voor analyse van ionische opgeloste stoffen
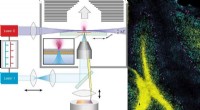
- Innovatieve methode geeft uniek inzicht in de structuur van cellen en weefsels
- Sinaasappelschilolie opzuigen tot nieuwe, aangename aromastoffen

- Topologiecontrole van menselijke fibroblastcellen monolaag door vloeibaar kristalelastomeer

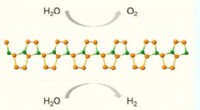
- Tijd voor een nieuwe concurrent in energieconversie en opslag
 Lost Oil Rubberhandschoenen op?
Lost Oil Rubberhandschoenen op?  Wat zijn 5 kenmerken die alle mineralen gemeen hebben?
Wat zijn 5 kenmerken die alle mineralen gemeen hebben?  Waar is lichaamsvet van gemaakt?
Waar is lichaamsvet van gemaakt?  Waarom is straling van de aardoppervlak en de atmosfeer belangrijk voor levende dingen?
Waarom is straling van de aardoppervlak en de atmosfeer belangrijk voor levende dingen?  Wat is een lysosoom dat bacterie eet of opneemt?
Wat is een lysosoom dat bacterie eet of opneemt?  Hoeveel protonen P en neutronen zijn er in een kern aanwezig PB van atomaire massa 206?
Hoeveel protonen P en neutronen zijn er in een kern aanwezig PB van atomaire massa 206?  Waarom maakt suikerwater dat is gemaakt voor kolibries winderig
Waarom maakt suikerwater dat is gemaakt voor kolibries winderig  Robots om het Great Barrier Reef te redden
Robots om het Great Barrier Reef te redden
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com


