
Wetenschap
Hoeveel mol bariumsulfaat wordt geproduceerd uit 0,100 molchloride?
* De reactie: We moeten de volledige chemische reactie weten met bariumchloride. Bijvoorbeeld:
* Reactie 1: Bacl₂ (aq) + na₂so₄ (aq) → baso₄ (s) + 2 NaCl (aq)
* Reactie 2: BACL₂ (aq) + h₂so₄ (aq) → baso₄ (s) + 2 hcl (aq)
* De beperkende reactant: Als we de reactie weten, moeten we ook de hoeveelheid van de andere reactant (zoals natriumsulfaat of zwavelzuur) kennen om de beperkende reactant te bepalen. De beperkende reactant bepaalt hoeveel product kan worden gevormd.
Hier is hoe u het probleem kunt oplossen zodra u de volledige informatie hebt:
1. Breng de chemische vergelijking in evenwicht: Zorg ervoor dat het aantal atomen van elk element hetzelfde is aan beide zijden van de vergelijking.
2. Identificeer de molverhouding: De evenwichtige vergelijking zal de verhouding van mol bariumchloride tot mol bariumsulfaat vertonen.
3. Bereken mol bariumsulfaat: Bereken met behulp van de molverhouding van stap 2 en de gegeven mol bariumchloride de mol bariumsulfaat geproduceerd.
Voorbeeld met reactie 1:
1. Balanced vergelijking: Bacl₂ (aq) + na₂so₄ (aq) → baso₄ (s) + 2 NaCl (aq)
2. Mol -verhouding: De vergelijking toont 1 mol BACL₂ produceert 1 mol baso₄.
3. mol Baso₄: Omdat de verhouding 1:1 is, zal 0,100 mol BACL₂ 0,100 mol produceren van Baso₄.
 Machine learning-innovatie om chemische bibliotheek voor medicijnontdekking te ontwikkelen
Machine learning-innovatie om chemische bibliotheek voor medicijnontdekking te ontwikkelen Biologische on-demand
Biologische on-demand Zullen lithium-luchtbatterijen ooit vliegen?
Zullen lithium-luchtbatterijen ooit vliegen? Wat is de chemische formule voor beryllium perbromaat?
Wat is de chemische formule voor beryllium perbromaat?  Vloeistof-vloeistof fasescheiding blijkt het proces van het omzetten van spidroïne-eiwitten in spinnenwebvezels te stimuleren
Vloeistof-vloeistof fasescheiding blijkt het proces van het omzetten van spidroïne-eiwitten in spinnenwebvezels te stimuleren
Hoofdlijnen
- Wat voor soort bacteriën is in antibiotica coccus bacillus of spirillum?
- Waar is het gen G verantwoordelijk voor bij deze fruitvliegjes?
- Welke voedingsstof wordt door bacteriën in verschillende vormen veranderd?
- Waarom worden eiwitten als organisch beschouwd?
- Wat is een in de wetenschap?
- Wat wordt bewaard in Gene Bank?
- Hoe zijn bloemen vergelijkbaar met de voortplantingsorganen van de plant?
- Waarom werden archaea en bacteriën tot voor kort gegroepeerd door biologen?
- Welk type cellulaire ademhaling vormt de meeste ATP?
- Katalysatorvervroeging verwijdert verontreinigende stoffen bij lage temperaturen

- Op weg naar de ontwikkeling van medicijnen voor aan veroudering gerelateerde ziekten
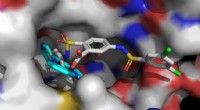
- Op de natuur geïnspireerd materiaal maakt gebruik van vloeibare versterking

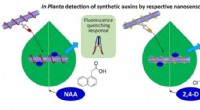
- Onderzoekers ontwerpen sensoren om plantenhormonen snel te detecteren
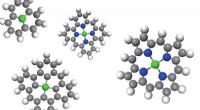
- Eenvoudige vergelijking leidt tot het creëren van schone-energiekatalysatoren
 Wat zijn de voor- en nadelen van ondergrondse mijnbouw?
Wat zijn de voor- en nadelen van ondergrondse mijnbouw?  Zullen cyborgs gemaakt worden van melanine? Pigmentdoorbraak maakt biocompatibele elektronica mogelijk
Zullen cyborgs gemaakt worden van melanine? Pigmentdoorbraak maakt biocompatibele elektronica mogelijk Nieuwe tool schat hoeveel betaalbare woningen een stad nodig heeft
Nieuwe tool schat hoeveel betaalbare woningen een stad nodig heeft Hoe warm weer of felle lichten de vergroening van bomen kunnen beïnvloeden
Hoe warm weer of felle lichten de vergroening van bomen kunnen beïnvloeden NASA-team kijkt eerst naar de oude aarde om wazige exoplaneten te bestuderen
NASA-team kijkt eerst naar de oude aarde om wazige exoplaneten te bestuderen Wie heeft zuurstoftanks uitgevonden?
Wie heeft zuurstoftanks uitgevonden?  Feminisering van wilde mannelijke forel in Denemarken blijkt om te keren
Feminisering van wilde mannelijke forel in Denemarken blijkt om te keren De chemische eigenschappen van materie komen meestal van?
De chemische eigenschappen van materie komen meestal van?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

