
Wetenschap
Welk type reactie reageert magnesiummetaal met waterstofchloride opgelost in water?
Dit is waarom:
* enkele verplaatsingsreacties Betrek het ene element dat een ander element in een verbinding vervangt.
* In dit geval is magnesium (mg) meer reactiever dan waterstof (H).
* Magnesium verplaatst waterstof uit zoutzuur (HCl), vormt magnesiumchloride (mgcl₂) en brengt waterstofgas vrij (H₂).
De evenwichtige chemische vergelijking voor deze reactie is:
mg (s) + 2HCl (aq) → mgcl₂ (aq) + h₂ (g)
Key Observations:
* Magnesiummetaal zal krachtig reageren en bubbels van waterstofgas produceren.
* De oplossing wordt warm vanwege de warmte die tijdens de reactie wordt vrijgegeven.
* De oplossing zal van kleur veranderen als magnesiumchloride oplost.
Laat het me weten als je meer details wilt over enkele verplaatsingsreacties!
 Is het combineren van koolstofdioxide en water om suiker te maken een fysieke verandering?
Is het combineren van koolstofdioxide en water om suiker te maken een fysieke verandering?  Wat is het voorbeeld van slechte effecten chemische veranderingen?
Wat is het voorbeeld van slechte effecten chemische veranderingen?  Cascades met kooldioxide
Cascades met kooldioxide Wat is de chemische vergelijking voor organische verbindingen?
Wat is de chemische vergelijking voor organische verbindingen?  Wat is een verbinding die bestaat uit kleine atoommassa die eerder nodig is?
Wat is een verbinding die bestaat uit kleine atoommassa die eerder nodig is?
 Hoe vertrouwen dieren en planten op elkaar?
Hoe vertrouwen dieren en planten op elkaar?  Welke lokale bevolking op aarde heeft het meest consistente en comfortabele klimaat?
Welke lokale bevolking op aarde heeft het meest consistente en comfortabele klimaat?  Simulaties tonen aan dat delen van Amazon tegen 2050 kunnen overschakelen van koolstofput naar koolstofbron
Simulaties tonen aan dat delen van Amazon tegen 2050 kunnen overschakelen van koolstofput naar koolstofbron Portugese brandweerlieden brengen bosbranden onder controle
Portugese brandweerlieden brengen bosbranden onder controle Wat is de betekenis van grondkwaliteit?
Wat is de betekenis van grondkwaliteit?
Hoofdlijnen
- Welk deel van DNA biedt de code voor eiwitten?
- Pesticiden kunnen ervoor zorgen dat hommels hun buzz verliezen, studie vondsten
- Wat is de celtheor?
- Wetenschappers ontdekken hoe het SARS-CoV-2-virus het replicatieprogramma in geïnfecteerde cellen initieert
- Cellen die ziekteverwekkers identificeren en van elkaar onderscheiden, wat wordt genoemd?
- De membraanreceptoren zijn eiwitten die zouden worden gesynthetiseerd op ribosomen waar?
- Kan B genotype trouwen met een a en o negatief produceren?
- Wetenschappers proberen oude slachtmethoden na te bootsen en leren hoe Neanderthalers vogels aten
- Eencellig onderzoek belicht de rol van DNA-methylatie bij beslissingen over het lot van cellen
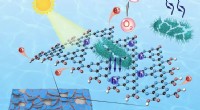
- Wetenschappers ontwikkelen metaalvrije fotokatalysator om pathogeenrijk water binnen enkele minuten te zuiveren
- Biochemische netwerken in kaart gebracht in de middendarm van Aedes aegypti-muggen

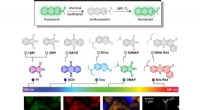
- Schakelaar met één atoom laadt fluorescerende kleurstoffen op
- Hoe groene algen hun enzymen samenstellen

- Onderzoekers verbeteren katalysator die voor altijd chemicaliën vernietigt met zonlicht

 Waarom is het belangrijk voor signaaltransductiesystemen om een snelle respons in cel te activeren en snel te kunnen afsluiten?
Waarom is het belangrijk voor signaaltransductiesystemen om een snelle respons in cel te activeren en snel te kunnen afsluiten?  As uit Alaska-vulkaan roept luchtvaartwaarschuwing op
As uit Alaska-vulkaan roept luchtvaartwaarschuwing op Elementen die worden gebruikt voor het maken van X-Rays
Elementen die worden gebruikt voor het maken van X-Rays Lipiden met potentiële gezondheidsvoordelen in kruidenthee geïdentificeerd
Lipiden met potentiële gezondheidsvoordelen in kruidenthee geïdentificeerd  Verkenning van oceaan en ruimte bij URIs Graduate School of Oceanography
Verkenning van oceaan en ruimte bij URIs Graduate School of Oceanography Welke factoren die de typen en het aantal organismen in een ecosysteem bepalen, worden genoemd?
Welke factoren die de typen en het aantal organismen in een ecosysteem bepalen, worden genoemd?  Beschadigd schip dat olie lekt voor Mauritius kan splitsen:PM
Beschadigd schip dat olie lekt voor Mauritius kan splitsen:PM In welke staat is 's werelds grootste olifantenfossiel?
In welke staat is 's werelds grootste olifantenfossiel?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

