
Wetenschap
Wat is een verbinding die bestaat uit kleine atoommassa die eerder nodig is?
Dit is waarom:
* kleinere atoomradius: Atomen met kleinere atoommassa's hebben over het algemeen kleinere atoomstralen. Dit betekent dat de elektronen dichter bij de kern zijn en een sterkere elektrostatische aantrekkingskracht ervaren.
* sterkere nucleaire trek: De kleinere afstand tussen de kern en elektronen leidt tot een sterkere aantrekkelijke kracht van de kern. Dit maakt het moeilijker om een elektron te verwijderen.
* Hogere ionisatie -energie: Ionisatie -energie is de energie die nodig is om een elektron uit een gasvormig atoom of ion te verwijderen. Vanwege de sterke aantrekkingskracht is meer energie nodig om de kracht te overwinnen die het elektron op zijn plaats houdt, wat resulteert in een hogere ionisatie -energie.
Voorbeeld:
Helium (hij) heeft een zeer kleine atoommassa en een zeer hoge ionisatie -energie in vergelijking met grotere atomen zoals kalium (K).
Laat het me weten als je nog andere vragen hebt!
 Hoe het risico op mislukking voor milieuprojecten te verminderen?
Hoe het risico op mislukking voor milieuprojecten te verminderen? Vissen met geweren op bedreigd meer in Kenia
Vissen met geweren op bedreigd meer in Kenia Voedselketens en hoe ze worden beïnvloed door waterverontreiniging
Voedselketens en hoe ze worden beïnvloed door waterverontreiniging  GPM ziet tropische cycloon Fakir ontstaan in de buurt van Madagascar
GPM ziet tropische cycloon Fakir ontstaan in de buurt van Madagascar Mogelijke onomkeerbare veranderingen in subsystemen voordat omslagpunten voor klimaatverandering worden bereikt
Mogelijke onomkeerbare veranderingen in subsystemen voordat omslagpunten voor klimaatverandering worden bereikt
Hoofdlijnen
- Het verwarmen van eiwitten om te begrijpen hoe genen werken
- Wat zijn feiten over wat een wetenschappers doen?
- Welke twee organellen zijn door endosymbiose onderdeel geworden van de eukaryote cel?
- Mutaties die willekeurig optreden worden genoemd?
- Waar staan de letters DNA voor?
- Hoe werken rode bloedcellen en botten samen?
- Wat is de oorsprong van frank?
- Onderzoek naar de genetica van macroalgen werpt licht op hoe zeewier meercellig werd
- Bloedmonsters tonen aan dat dodelijke kikkerschimmel in het wild aan het werk is
- Een doorbraak in katalysatoren:kleiner dan nanoschaal

- Wetenschappers maken waterfiltratiemembranen die zichzelf kunnen reinigen

- Nieuw inzicht in de mechanica van het rotavirus kan leiden tot verbeterde behandelingen

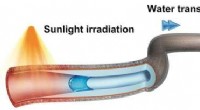
- Snel gecontroleerd transport van waterdruppels door door zonlicht aangedreven pomp
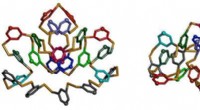
- Zelfgebouwde gevouwen macrocycles maken met lage symmetrie
 Wat voor soort symbiose bestaat er tussen gras en migrerende dieren?
Wat voor soort symbiose bestaat er tussen gras en migrerende dieren?  Hoe Zweden van de minst democratische naar de verzorgingsstaat ging
Hoe Zweden van de minst democratische naar de verzorgingsstaat ging Afscheid nemen van plakkerig ijs, maar dan met een korreltje zout
Afscheid nemen van plakkerig ijs, maar dan met een korreltje zout  Nanodeeltjes geassembleerd in tumoren vangen medicijnen en beeldvormende middelen op
Nanodeeltjes geassembleerd in tumoren vangen medicijnen en beeldvormende middelen op Effecten van autovervuiling
Effecten van autovervuiling Het kleinste sanitair ter wereld kan ooit medicijnen naar individuele menselijke cellen leiden
Het kleinste sanitair ter wereld kan ooit medicijnen naar individuele menselijke cellen leiden Welke manier bewegen rotsen in een fout?
Welke manier bewegen rotsen in een fout?  Hoe het creëren van minder gasachtige koeien de klimaatverandering kan helpen bestrijden
Hoe het creëren van minder gasachtige koeien de klimaatverandering kan helpen bestrijden
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

