
Wetenschap
Wat is het verschil tussen aluminiumsulfide en sulfaat?
aluminium sulfide (al₂s₃)
* Samenstelling: Twee aluminium (AL) atomen en drie zwavel (s) atomen.
* ionische verbinding: Aluminium is een metaal en zwavel is een niet -metaal, dus ze vormen een ionische binding.
* eigenschappen:
* Witte kristallijne vaste stof
* Zeer reactief met water, die waterstofsulfidegas (H₂S) produceert, die een sterke rotte eiergeur heeft.
* Gebruikt in sommige chemische reacties en bij de productie van andere aluminiumverbindingen.
aluminiumsulfaat (Al₂ (So₄) ₃)
* Samenstelling: Twee aluminium (AL) atomen en drie sulfaat (SO₄) ionen.
* ionische verbinding: Aluminium is een metaal en de sulfaatgroep (SO₄) is een polyatomisch ion, dus ze vormen een ionische binding.
* eigenschappen:
* Witte kristallijne vaste stof
* Oplosbaar in water
* Gebruikt in verschillende toepassingen:
* Waterbehandeling (coagulatie)
* Papermaking
* Brandvertragers
* Textielverven
Belangrijkste verschillen:
* anion: Aluminiumsulfide bevat sulfide -ionen (s²⁻), terwijl aluminiumsulfaat sulfaationen bevat (SO₄²⁻).
* Reactiviteit met water: Aluminiumsulfide reageert gewelddadig met water, terwijl aluminiumsulfaat oplost in water.
* Toepassingen: Hun gebruik is heel anders en weerspiegelen hun verschillende chemische eigenschappen.
Laat het me weten als je nog meer vragen hebt!
 De term evolutie kan het beste worden beschreven als?
De term evolutie kan het beste worden beschreven als?  Argentijns moerasland bedreigd door ergste branden in decennia
Argentijns moerasland bedreigd door ergste branden in decennia Hittegolf Europa breekt Belgisch record kwik om meer te stijgen
Hittegolf Europa breekt Belgisch record kwik om meer te stijgen Wat is het belangrijke fysieke kenmerk van Australië?
Wat is het belangrijke fysieke kenmerk van Australië?  Nieuw rapport toont aan dat de gevaren van luchtvervuiling landelijk blijven bestaan
Nieuw rapport toont aan dat de gevaren van luchtvervuiling landelijk blijven bestaan
Hoofdlijnen
- Welke wetenschappers gebruiken om te classificeren?
- Wat gebruiken wetenschappers om dieren in dezelfde familie te classificeren?
- Welke studie helpt je om de redenering van de redenering te begrijpen?
- Wat deed Mendel om ervoor te zorgen dat de planten in zijn experimenten bestoven en niet zelf bestuiven?
- Welke dieren zijn voorbeelden van herbivoren?
- Hoe cranberrymoerassen werken
- Toenemende haaienwaarnemingen aan de oostkust hebben strandwachten paraat en experts zoeken naar antwoorden
- De wilde ezel keert terug
- Wat is de wetenschappelijke naam voor hond in Phylum?
- Sandia identificeert ongebruikelijke polycyclische aromatische koolwaterstoffen met behulp van tandem-massaspectrometrie

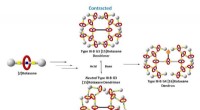
- Doorbraak in macromoleculaire machines voor actief gecontroleerde toediening van kankergeneesmiddelen
- Oleo Sponge succesvol in echte omstandigheden voor de kust van Californië

- Hoe maak je het gemakkelijker om plantaardig afval om te zetten in biobrandstoffen?

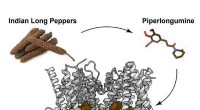
- Ingrediënt in Indiase lange peper veelbelovend tegen hersenkanker in diermodellen
 Onderzoek naar stikstoffixatie kan licht werpen op biologisch mysterie
Onderzoek naar stikstoffixatie kan licht werpen op biologisch mysterie Wat is de rol van mRNA en tRNA in productie -eiwit?
Wat is de rol van mRNA en tRNA in productie -eiwit?  Wat doet ADP in de biologie?
Wat doet ADP in de biologie?  Welk type rots wordt langzaam begraven sedimenten die later werden gecementeerd door opgeloste minerials?
Welk type rots wordt langzaam begraven sedimenten die later werden gecementeerd door opgeloste minerials?  Herziening van multiferroics voor de toekomst, energiezuinige gegevensopslag
Herziening van multiferroics voor de toekomst, energiezuinige gegevensopslag Wat doet de zuurgraad ons mensen?
Wat doet de zuurgraad ons mensen?  Waarom verdwijnt de maan uit het zicht tijdens een eclips?
Waarom verdwijnt de maan uit het zicht tijdens een eclips?  Als er intelligente buitenaardse wezens bestaan, waarom hebben we ze dan niet gezien?
Als er intelligente buitenaardse wezens bestaan, waarom hebben we ze dan niet gezien?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

