
Wetenschap
Wat betekent een geconcentreerd zwak zuur?
Hoewel een geconcentreerd zwak zuur een hoge concentratie zuurmoleculen heeft, heeft het nog steeds een lage dissociatieconstante. Dit betekent dat slechts een klein deel van de zuurmoleculen daadwerkelijk dissocieert in water. Het merendeel van de zuurmoleculen blijft ongedissocieerd en daarom heeft de oplossing een lage pH.
Zoutzuur (HCl) is bijvoorbeeld een sterk zuur dat volledig dissocieert in water. Dit betekent dat alle HCl-moleculen in oplossing dissociëren in H+ en Cl-ionen. De dissociatieconstante voor HCl is zeer hoog, wat betekent dat het een zeer sterk zuur is.
Aan de andere kant is azijnzuur (CH3COOH) een zwak zuur dat slechts gedeeltelijk dissocieert in water. Dit betekent dat slechts een klein deel van de CH3COOH-moleculen in oplossing dissociëren in H+- en CH3COO--ionen. De dissociatieconstante voor azijnzuur is erg laag, wat betekent dat het een zeer zwak zuur is.
Hoewel azijnzuur een zwak zuur is, kan het nog steeds geconcentreerd zijn. Dit betekent dat het een hoge concentratie CH3COOH-moleculen in oplossing kan hebben. Zelfs bij hoge concentraties zal azijnzuur echter nog steeds slechts gedeeltelijk dissociëren in water. Dit betekent dat de oplossing een lage pH zal hebben.
 Materiaal verandert van kleur, afhankelijk van hoe je ernaar kijkt
Materiaal verandert van kleur, afhankelijk van hoe je ernaar kijkt  Wat is een thermoplastisch polymeer?
Wat is een thermoplastisch polymeer?  Wat zijn de natuurlijke bronnen van kaliumhydroxide?
Wat zijn de natuurlijke bronnen van kaliumhydroxide?  Wanneer kaliumbromaat wordt verwarmd, valt het uiteen in bromide. Welke gasreactie vindt er plaats?
Wanneer kaliumbromaat wordt verwarmd, valt het uiteen in bromide. Welke gasreactie vindt er plaats?  Chemici bedenken een eenvoudigere nieuwe methode voor het maken van een algemeen type bouwsteen voor medicijnen
Chemici bedenken een eenvoudigere nieuwe methode voor het maken van een algemeen type bouwsteen voor medicijnen
 Soldaten ingezet om bosbranden in Engeland te bestrijden
Soldaten ingezet om bosbranden in Engeland te bestrijden Wetenschappers werken samen om aan te tonen dat de biodiversiteit in bossen op meer dan één manier groen is
Wetenschappers werken samen om aan te tonen dat de biodiversiteit in bossen op meer dan één manier groen is  Is het beleid ter bevordering van het fietsgebruik maatschappelijk rendabel?
Is het beleid ter bevordering van het fietsgebruik maatschappelijk rendabel? Wetenschappers kweken supervoedzame gewassen om honger in de wereld te helpen oplossen
Wetenschappers kweken supervoedzame gewassen om honger in de wereld te helpen oplossen Turbulentie-expert onthult kosten klimaatverandering voor luchtvaartverzekeraars
Turbulentie-expert onthult kosten klimaatverandering voor luchtvaartverzekeraars
Hoofdlijnen
- Bevat osmose aminozuren of suiker?
- Hoe vogelvoeders kleine soorten helpen infecties te bestrijden
- Hoe heet het proces waarbij een bacteriële cel DNA opneemt dat door anderen wordt vrijgegeven?
- Antimicrobieel peptide van koeien toont potentieel voor de behandeling van hypervirulente bacteriën
- Vertoonen stadsvissen een verminderde slaap?
- Kan een criticus die een gelovige is geworden, anderen beïnvloeden? Het geval van genetisch gemodificeerd voedsel
- Hoe een filmmaker, een stapel oude schelpen en een stel amateurs de oesterriffen van Australië terugbrengen
- Nieuwe hulpmiddelen onthullen hoe genen werken en cellen zich organiseren
- Onderzoek onderzoekt hoe de oppervlakken van borstimplantaten de immuunrespons beïnvloeden
- Nieuwe 3D-printtechniek produceert levende 4D-materialen

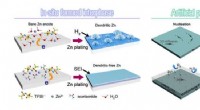
- Interfaciale chemie verbetert de oplaadbaarheid van Zn-batterijen
- De bidsprinkhaangarnalen perfect schild

- De leiding nemen om de juiste balans te vinden voor geavanceerde opto-elektronische apparaten

- Het creëren van lithium-ionbatterijen met een hogere energiedichtheid voor toepassingen op het gebied van hernieuwbare energie

 Kenmerken van een jakhals
Kenmerken van een jakhals  Cichlidenvissen uit het Afrikaanse Tanganyikameer werpen licht op hoe de diversiteit van organismen ontstaat
Cichlidenvissen uit het Afrikaanse Tanganyikameer werpen licht op hoe de diversiteit van organismen ontstaat  Extreme stroomuitval door ruimteweer kan de VS meer dan $ 40 miljard per dag kosten
Extreme stroomuitval door ruimteweer kan de VS meer dan $ 40 miljard per dag kosten Bergleeuw! Staan of rennen?
Bergleeuw! Staan of rennen?  Studie zegt dat verzekeringssector gevaarlijk onvoorbereid is op extreem weer
Studie zegt dat verzekeringssector gevaarlijk onvoorbereid is op extreem weer Waymo-chef zegt dat zijn technologie een fatale Uber-crash zou hebben voorkomen
Waymo-chef zegt dat zijn technologie een fatale Uber-crash zou hebben voorkomen Extreemrechts geweld in Portugal put kracht uit skinhead-wortels - studie
Extreemrechts geweld in Portugal put kracht uit skinhead-wortels - studie NASA CubeSat test geminiaturiseerde weersatelliettechnologie
NASA CubeSat test geminiaturiseerde weersatelliettechnologie
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

