
Wetenschap
Welk element is het meest reactieve stikstofzuurstoffluor neon en waarom?
* elektronegativiteit: Fluor heeft de hoogste elektronegativiteit van alle elementen. Dit betekent dat het een sterke aantrekkingskracht heeft op elektronen.
* Elektronenaffiniteit: Fluorine heeft ook een zeer hoge elektronenaffiniteit, wat betekent dat het een grote hoeveelheid energie vrijgeeft wanneer het een elektron krijgt.
* Kleine atoommaat: Fluor heeft een kleine atoomradius, waardoor zijn kern een sterke trek van elektronen kan uitoefenen.
Deze factoren gecombineerd maken fluor zeer reactief. Het vormt gemakkelijk verbindingen met andere elementen, vaak door elektronen er vanaf te trekken.
Hier is een vergelijking van de andere elementen:
* zuurstof: Hoewel reactief is, is zuurstof minder reactief dan fluor. Het heeft een lagere elektronegativiteit en elektronenaffiniteit.
* stikstof: Stikstof is relatief niet -reactief vanwege de sterke drievoudige binding tussen zijn atomen.
* neon: Neon is een edelgas en is extreem niet -reactief. De buitenste elektronenschaal is volledig gevuld, waardoor het stabiel en bestand is tegen het vormen van bindingen.
 Watertekort? Laat Lasso een ijsberg
Watertekort? Laat Lasso een ijsberg  koude temperaturen, stroomuitval leidt tot waterproblemen
koude temperaturen, stroomuitval leidt tot waterproblemen Antarctische landschapsinzichten houden voorspellingen over ijsverlies op de radar
Antarctische landschapsinzichten houden voorspellingen over ijsverlies op de radar Onderscheid maken tussen voor- en naschokken van aardbevingen
Onderscheid maken tussen voor- en naschokken van aardbevingen Wiskundig model voorspelt de beweging van microplastics in de oceaan
Wiskundig model voorspelt de beweging van microplastics in de oceaan
Hoofdlijnen
- Wat is het doel van DNA -sequencing?
- Waarom zouden wetenschappers communiceren met andere wetenschappers?
- Hoe heet de studie van een fysieke structuur van mensen of andere dieren?
- Kan klimaatverandering onvruchtbaarheid veroorzaken?
- Noem de delen van een angiosperm -bloem waarin de mannelijke en vrouwelijke gametofyt plaatsvindt?
- Een voorbeeld van een biologische universele gebeurtenis die zich op relatief tegelijkertijd in alle samenlevingen voordoet, wordt wat genoemd?
- Wat is een basiseenheid van structuur en functie gevonden in alle Ilvung -dingen?
- Soorten organismen die van plantencellen zijn gemaakt
- Welke alleen bepaalde materialen kunnen de cel binnenkomen?
- Onthulling van de nare werking van transvetzuren in het bloed

- Onderzoeksgroep gebruikt supercomputing om zich te richten op de meest veelbelovende kandidaat-geneesmiddelen uit een enorm aantal mogelijkheden
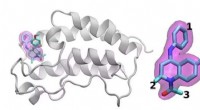
- Ontdekken hoe het toevoegen van UV-behandeling aan waterchlorering de productie van giftige trihalomethaan daadwerkelijk kan verhogen

- Melkeiwit kan de gezondheid van bosbessen helpen verbeteren

- Onderzoekers rapporteren nieuwe toestand van materie beschreven als vloeibaar glas

 Wat is de procentuele samenstelling van calciumfluoride?
Wat is de procentuele samenstelling van calciumfluoride?  Van vloeistof naar vast:hoe lang duurt het voordat water bevriest?
Van vloeistof naar vast:hoe lang duurt het voordat water bevriest?  Hoe lang zou het duren om door het heelal te lopen?
Hoe lang zou het duren om door het heelal te lopen?  Waarom zijn decomposers essentieel voor de creatie?
Waarom zijn decomposers essentieel voor de creatie?  Wat gebeurt er bij een zuurgebaseerde reactie volgens de Arrhenius-definitie?
Wat gebeurt er bij een zuurgebaseerde reactie volgens de Arrhenius-definitie?  Wanneer denken consumenten dat een freebie waardevoller is dan een afgeprijsd product?
Wanneer denken consumenten dat een freebie waardevoller is dan een afgeprijsd product?  Hoe een verbod op positieve actie selectieve hogescholen en het personeelsbestand minder divers maakt
Hoe een verbod op positieve actie selectieve hogescholen en het personeelsbestand minder divers maakt Wat is een vloeibare brandstof afgeleid van plantaardige materialen?
Wat is een vloeibare brandstof afgeleid van plantaardige materialen?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

