
Wetenschap
Vormt fluor ionische of covalente bindingen?
Dit is waarom:
* elektronegativiteit: Fluor is het meest elektronegatieve element, wat betekent dat het een sterke aantrekkingskracht heeft op elektronen. Hoewel het elektronen van andere atomen kan aantrekken, is het niet sterk genoeg om een elektron volledig te stelen om een echte ionische binding te vormen.
* klein formaat: Fluor is erg klein, wat betekent dat de kern een sterke trek van gedeelde elektronen kan uitoefenen. Dit maakt het waarschijnlijker dat het elektronen delen in plaats van ze volledig te winnen.
Het is echter vermeldenswaard dat fluor soms ionische bindingen kan vormen met zeer elektropositieve elementen, zoals alkali -metalen (bijvoorbeeld lithiumfluoride, LIF). Dit komt omdat het verschil in elektronegativiteit zo groot is dat de binding meer ionisch van karakter wordt.
Samenvattend vormt fluor meestal covalente bindingen vanwege de hoge elektronegativiteit en kleine omvang, maar het kan in sommige extreme gevallen ionische bindingen vormen met zeer elektropositieve elementen.
 Veelzijdige chemoproteomische probes voor op activiteit gebaseerde eiwitprofilering
Veelzijdige chemoproteomische probes voor op activiteit gebaseerde eiwitprofilering Wat zijn fluorescerende pigmenten en wat is de chemische samenstelling?
Wat zijn fluorescerende pigmenten en wat is de chemische samenstelling?  Xenon verbetert de eigenschappen van maxillofaciale en orthopedische implantaten
Xenon verbetert de eigenschappen van maxillofaciale en orthopedische implantaten Wat zijn stabiele elementen?
Wat zijn stabiele elementen?  Is H2O warm water en CO2 koud water?
Is H2O warm water en CO2 koud water?
Hoofdlijnen
- Waarom kun je zeggen dat biologie leven en biologie is?
- Waar vind je een wetenschappelijk laboratorium dat de ziekte van Alzheimer bestudeert?
- Versteende cirkels in het zand aan de Zuid-Afrikaanse kust zijn mogelijk kunstwerken van onze vroege voorouders
- Hoe produceren niet -vasculaire planten voedsel?
- Wat is de functie van microbiologie?
- Wilde vissen gedijen ondanks hopeloze monstermutaties, volgens onderzoek
- Maïsplaag maakt gebruik van plantafweerstoffen om zichzelf te beschermen
- Bomen op een universiteitscampus doorstaan droogte dankzij lekkende leidingen
- Hoe stel je wetenschappelijke vragen?
- Onderzoek naar de neurologische impact van luchtvervuiling

- Traditionele eutectische legering biedt nieuwe hoop voor metaal-zuurstofbatterijen met hoge energiedichtheid

- Genetica-inspanningen die de voeding van popcorn verrijken, sorghum

- Ingenieurs identificeren verbeterde membranen om CO2 af te vangen bij kolencentrales

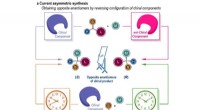
- Onderzoekers hebben toegang tot beide enantiomeren door de reactietijd te variëren
 Orbital lanceert dinsdag vracht naar ruimtestation
Orbital lanceert dinsdag vracht naar ruimtestation Eerste gecertificeerde referentiemateriaal voor analyse van nanodeeltjesgrootte
Eerste gecertificeerde referentiemateriaal voor analyse van nanodeeltjesgrootte Wat was de grootste verandering in de atmosfeer tussen Precambrian en Paleozoïsche tijdperken?
Wat was de grootste verandering in de atmosfeer tussen Precambrian en Paleozoïsche tijdperken?  Bioactieve natuurlijke verbindingen voor de strijd tegen kanker
Bioactieve natuurlijke verbindingen voor de strijd tegen kanker Video:Gallium en de geschiedenis van het periodiek systeem
Video:Gallium en de geschiedenis van het periodiek systeem Hoeveel regenwoud hebben vogels nodig?
Hoeveel regenwoud hebben vogels nodig?  Maanlasers en kosmische gewassen:NASA financiert UArizona-ruimteverkenningsmissies
Maanlasers en kosmische gewassen:NASA financiert UArizona-ruimteverkenningsmissies Wat is het gevolg van sedimentafzettingen?
Wat is het gevolg van sedimentafzettingen?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

