
Wetenschap
Waarom bestaat stikstof pentafluoride niet?
Hier is een uitsplitsing:
* Elektronische configuratie van stikstof: Stikstof heeft 5 valentie -elektronen. Om vijf obligaties te vormen, zou het zijn octet moeten uitbreiden om 10 elektronen te huisvesten. Stikstof breidt zijn octet echter niet gemakkelijk uit dan acht elektronen. Dit komt omdat de 2P -orbitalen de enige zijn die beschikbaar zijn voor binding en ze kunnen slechts maximaal acht elektronen bevatten.
* sterische hindering: Zelfs als stikstof zijn octet zou kunnen uitbreiden, zouden de vijf fluoratomen extreem druk zijn rond het stikstofatoom. Deze ernstige sterische belemmering zou het molecuul zeer onstabiel maken en waarschijnlijk ontleden.
Alternatieve verbindingen:
Hoewel NF5 niet stabiel is, bestaan er andere stikstoffluoriden, zoals stikstof trifluoride (NF3), wat een stabiele verbinding is.
Samenvattend: Stikstof pentafluoride is geen levensvatbare verbinding vanwege beperkingen in de elektronische configuratie van stikstof en significante sterische hindering.
 Wat is heterogene katalyse en oppervlaktewetenschappelijke groep?
Wat is heterogene katalyse en oppervlaktewetenschappelijke groep?  Hoeveel mol N2 zijn er bij een temperatuur 20 graden Celsius 1 atm druk als het gas 44 liter bezet?
Hoeveel mol N2 zijn er bij een temperatuur 20 graden Celsius 1 atm druk als het gas 44 liter bezet?  Wat gebeurt er met de waterstofbruggen als water smelt?
Wat gebeurt er met de waterstofbruggen als water smelt?  Nieuwe lijm kan miljoenen medische procedures veiliger maken, minder invasief voor patiënten
Nieuwe lijm kan miljoenen medische procedures veiliger maken, minder invasief voor patiënten Bereken verdunningsoplossingen
Bereken verdunningsoplossingen
 Wetenschappers identificeren hoe de ontleding van Arctische landschappen verandert door de steeds snellere klimaatverandering
Wetenschappers identificeren hoe de ontleding van Arctische landschappen verandert door de steeds snellere klimaatverandering  Terwijl de droogte in Kaapstad toeslaat, wat is dag nul?
Terwijl de droogte in Kaapstad toeslaat, wat is dag nul? Jota, verzwakt maar dodelijk, scheurt door Midden-Amerika
Jota, verzwakt maar dodelijk, scheurt door Midden-Amerika Warmere temperaturen veroorzaken een afname van de belangrijkste afvoermaatregel
Warmere temperaturen veroorzaken een afname van de belangrijkste afvoermaatregel Feiten over de wandelstok bug
Feiten over de wandelstok bug
Hoofdlijnen
- Wat is de inhoud van de cel?
- Nieuwe theorie daagt de huidige kijk uit op hoe de hersenen langetermijngeheugen opslaan
- Welk schip bevat sluitspier?
- Nieuwe studie onderzoekt hoe overtuigingen en politieke voorkeuren het begrip van het publiek over raciale ongelijkheid vormen
- Wat zijn enkele pakkende wetenschapsprojecttitels voor het immuunsysteem?
- Stelen nucleïnezuren op en geven ze erfelijke informatie over?
- Hoeveel vellen papier kunnen uit één enkele boom worden geproduceerd?
- Cellen zijn essentieel voor elke vorm van?
- Er wordt een verrassende nieuwe vlindervis beschreven uit de Filippijnse schemerzone en tentoonstelling
- Net als Wolverine, mensen hebben metaal nodig om sterke botten te behouden

- Een nieuwe methode voor proximity-labeling op nanometerschaal die zich richt op histidine-residuen

- De vloeibare assemblagelijn van ingenieurs maakt microdeeltjes van medicijnen duizend keer sneller dan ooit tevoren

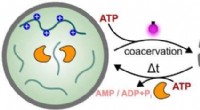
- Hoe licht kan worden gebruikt om processen in synthetische cellen te controleren
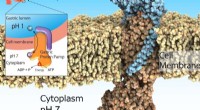
- Onderzoekers stellen kristalstructuur van maagprotonpomp vast
 Soorten liften mee op vogels en de wind om zich bij groene dakgemeenschappen aan te sluiten
Soorten liften mee op vogels en de wind om zich bij groene dakgemeenschappen aan te sluiten Hoe glycolyse aan kinderen te leren
Hoe glycolyse aan kinderen te leren New Horizons maakt eerste detectie van voorbijvliegend doel Kuipergordel
New Horizons maakt eerste detectie van voorbijvliegend doel Kuipergordel NY Times beëindigt afzonderlijke Spaanstalige operatie
NY Times beëindigt afzonderlijke Spaanstalige operatie Een krachtig leidend principe voor topologische kwantumsynthese
Een krachtig leidend principe voor topologische kwantumsynthese Nieuw inzicht in de oorsprong van water op aarde
Nieuw inzicht in de oorsprong van water op aarde Hoe werkt ruw ER met Ribosomes?
Hoe werkt ruw ER met Ribosomes?  John Dalton combineerde het idee van leeg met Griekse theorie -atoom?
John Dalton combineerde het idee van leeg met Griekse theorie -atoom?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

