
Wetenschap
Hoe bindt u covalent aluminium en zwavel?
Uitdagingen:
* elektronegativiteit: Aluminium (AL) is een metaal met relatief lage elektronegativiteit, terwijl zwavel (s) een niet -metaal is met hoge elektronegativiteit. Dit verschil maakt hen waarschijnlijker om ionische bindingen te vormen, waarbij elektronen worden overgedragen, in plaats van covalente bindingen, waarbij elektronen worden gedeeld.
* de voorkeur van aluminium: Aluminium geeft meestal de voorkeur aan ionische bindingen met niet -metalen.
Hoe ze binden:
* Hoge temperaturen: Covalente binding tussen aluminium en zwavel kan optreden bij zeer hoge temperaturen (meer dan 1000 ° C). Onder deze extreme omstandigheden delen de aluminiumatomen vaker elektronen met zwavelatomen.
* Specifieke voorwaarden: Aluminiumsulfide (Al₂s₃) kan zich vormen als een vaste verbinding onder de juiste omstandigheden. Het is echter vaak onstabiel en heeft de neiging terug te ontleden in zijn elementen.
Het resultaat:
De covalente binding tussen aluminium en zwavel in Al₂s₃ wordt beschouwd als polaire covalent . Dit betekent dat de gedeelde elektronen niet gelijk worden gedeeld en het zwavelatoom een enigszins negatieve lading zal hebben, terwijl het aluminiumatoom een enigszins positieve lading zal hebben.
Belangrijke opmerking:
* De vorming van covalente bindingen tussen aluminium en zwavel is een complex proces dat specifieke voorwaarden vereist.
* In de meeste gevallen leidt de interactie tussen aluminium en zwavel tot de vorming van ionische verbindingen.
Laat het me weten als je meer wilt weten over specifieke reactieomstandigheden of eigenschappen van aluminiumsulfide!
 Het maken van maandverband van vetplanten zou de toegang tot sanitaire producten kunnen verbeteren
Het maken van maandverband van vetplanten zou de toegang tot sanitaire producten kunnen verbeteren  Wat komt na 3p in het atoom orbitaal?
Wat komt na 3p in het atoom orbitaal?  Hoeveel atomen zitten er in C6H4Cl2?
Hoeveel atomen zitten er in C6H4Cl2?  Dubbel gedoteerde koolstofmicrosferen met sterk stikstof en zwavel voor supercondensatoren
Dubbel gedoteerde koolstofmicrosferen met sterk stikstof en zwavel voor supercondensatoren Wetenschappers ontwikkelen een nieuw moleculair systeem gemaakt van het overvloedige element mangaan voor foto-oxidatie
Wetenschappers ontwikkelen een nieuw moleculair systeem gemaakt van het overvloedige element mangaan voor foto-oxidatie
 Hoe eetbare bessen te identificeren
Hoe eetbare bessen te identificeren  Historische hittegolf ontploft in het noordwesten terwijl het risico op bosbranden toeneemt
Historische hittegolf ontploft in het noordwesten terwijl het risico op bosbranden toeneemt De meeste plantenwortels groeien in welke horizon?
De meeste plantenwortels groeien in welke horizon?  Oceanografen leggen de relatie tussen grootte en productiviteit bloot in een van 's werelds meest complexe ecosystemen
Oceanografen leggen de relatie tussen grootte en productiviteit bloot in een van 's werelds meest complexe ecosystemen Wat dieren graven in de nacht?
Wat dieren graven in de nacht?
Hoofdlijnen
- Hoe vindt een mobiele DNA-sequentie zijn doelwit?
- Wat is een systeem dat bestaat uit de darmen en longen van de nieren leverhuid en longen zuivert het lichaam door afvalmateriaal te elimineren?
- Wat doet het celmembraan bij een dier?
- Hoe cellen door het plakkerigste slijm heen ritsen
- Prokaryotische celstructuur
- Waarom worden introns gekopieerd en vervolgens verwijderd uit de RNA -sequentie?
- Wat was er eerst:het hoofd of de hersenen?
- Lijst met toepassingen van elektroforese
- Wat is de betekenis van algemene wetenschap?
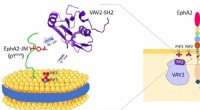
- Wetenschappers onthullen dubbele specificiteit van Vav2-SH2-eiwit
- Onderzoekers creëren kunstkraakbeen dat zichzelf kan herstellen

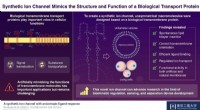
- Wetenschappers synthetiseren nieuwe kunstmatige moleculen die een celmembraaneiwit nabootsen
- Tandemkatalyse verbetert selectieve oxidatie van methaan tot oxygenaten
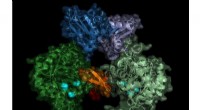
- Onderzoeksteam vindt mogelijke nieuwe aanpak voor medicijnen tegen slaapziekte
 Welk type binding wordt gevormd tussen fluor en silicium?
Welk type binding wordt gevormd tussen fluor en silicium?  De grote glasdominantie van Amerika hangt af van het lot van twee krachtige nieuwe telescopen
De grote glasdominantie van Amerika hangt af van het lot van twee krachtige nieuwe telescopen  Milieuwetenschappers nieuwe ozonisatiemethode behandelt water van antibioticaresiduen
Milieuwetenschappers nieuwe ozonisatiemethode behandelt water van antibioticaresiduen Ultragevoelige moleculaire detectie met synthetisering van golven met complexe frequenties
Ultragevoelige moleculaire detectie met synthetisering van golven met complexe frequenties  Gigantische lavakoepel bevestigd in de Japanse Kikai Caldera
Gigantische lavakoepel bevestigd in de Japanse Kikai Caldera Leren hoe kleding wordt gemaakt heeft een 'transformatief' effect op de relatie van mensen met fast fashion
Leren hoe kleding wordt gemaakt heeft een 'transformatief' effect op de relatie van mensen met fast fashion  Prehistorische tanden geven hun geheimen prijs
Prehistorische tanden geven hun geheimen prijs Vreemde zijde:waarom abseilende spinnen niet uit de hand lopen
Vreemde zijde:waarom abseilende spinnen niet uit de hand lopen
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

