
Wetenschap
Welk type binding wordt gevormd tussen fluor en silicium?
Dit is waarom:
* elektronegativiteit: Fluor is het meest elektronegatieve element, terwijl silicium een aanzienlijk lagere elektronegativiteit heeft. Dit betekent dat fluor een sterke aantrekkingskracht heeft op elektronen.
* Elektronen delen: Om een stabiele elektronenconfiguratie te bereiken, heeft fluor nog een elektron nodig en heeft silicium er vier nodig. Ze delen elektronen in een covalente binding, waarbij beide atomen elektronen bijdragen om een gedeeld paar te vormen.
* polariteit: Hoewel de binding covalent is, resulteert het grote verschil in elektronegativiteit tussen fluor en silicium in een polaire covalente binding . De gedeelde elektronen besteden meer tijd dichter bij het fluoratoom, waardoor het een gedeeltelijke negatieve lading en silicium een gedeeltelijke positieve lading krijgt.
 Wat is de dampdruk van propaan bij 15,0 graden C?
Wat is de dampdruk van propaan bij 15,0 graden C?  Is ammoniumnitriet zuur of basisch?
Is ammoniumnitriet zuur of basisch?  Waarom is het beter om propaan in vloeistoffen te transporteren en niet in gas?
Waarom is het beter om propaan in vloeistoffen te transporteren en niet in gas?  Vaccin-ingrediënten kunnen zich verbergen in bibliotheken met kleine moleculen
Vaccin-ingrediënten kunnen zich verbergen in bibliotheken met kleine moleculen Wat is de gelijkenis en het verschil tussen zwavellithium?
Wat is de gelijkenis en het verschil tussen zwavellithium?
 Wat is vervuiling die afkomstig is van slechts één bron die wordt genoemd?
Wat is vervuiling die afkomstig is van slechts één bron die wordt genoemd?  Wat gebeurt er als de Antarctische ijskap gedestabiliseerd raakt?
Wat gebeurt er als de Antarctische ijskap gedestabiliseerd raakt? Veengebieden zullen meer koolstof opslaan naarmate de planeet opwarmt
Veengebieden zullen meer koolstof opslaan naarmate de planeet opwarmt Biotische componenten van ecosystemen
Biotische componenten van ecosystemen  Wat voor de grond weg te dragen van de ene plaats naar de andere?
Wat voor de grond weg te dragen van de ene plaats naar de andere?
Hoofdlijnen
- Welke tak van de wetenschap vormt een veelbelovende carrièrepad?
- Welke suiker onderscheidt zich van DNA en RNA?
- Wat is er verschillen tussen de aminozuursequenties van hemoglobine bij mensen en kikkers?
- Achter de puppy-hondenogen
- Waarom zijn meiose en mitose verward?
- Welke theorie werd ontwikkeld rond het idee dat sommige eukaryotische organellen zijn geëvolueerd uit proyarotische organismen?
- Hoe kan de evolutionaire geschiedenis van een soort worden weergegeven?
- Is het waar of onwaar dat metabolische processen zuurstof vereisen anaërobe worden genoemd?
- Leven in drijfhout in zee:het geval van drijfhoutspecialist talitrids
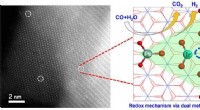
- Wetenschappers stellen redoxmechanisme voor water-gasverschuivingsreactie voor
- Overlevingsstrategie:hoe één enzym bacteriën helpt herstellen van blootstelling aan antibiotica

- Waterstofbindingen voor het eerst direct gedetecteerd

- Onderzoek onthult een nieuwe manier om chirale katalysatoren te maken

- Infraroodsensor dient als een nieuw hulpmiddel voor het ontdekken van medicijnen

 Hoeveel kracht is er nodig om een steen met een massa van 345 kg over 28 meter te verplaatsen terwijl hij 1008 J arbeid verricht?
Hoeveel kracht is er nodig om een steen met een massa van 345 kg over 28 meter te verplaatsen terwijl hij 1008 J arbeid verricht?  Wat is de meting van theormeter?
Wat is de meting van theormeter?  Wat stellen wetenschappers voor en testen om tot een oplossing te komen?
Wat stellen wetenschappers voor en testen om tot een oplossing te komen?  Wat zijn de transformaties van energie die plaatsvinden als je een lucifer aansteekt en vervolgens een kaars aansteekt?
Wat zijn de transformaties van energie die plaatsvinden als je een lucifer aansteekt en vervolgens een kaars aansteekt?  Hoe origami ziektediagnoses kan bepalen
Hoe origami ziektediagnoses kan bepalen  Hoe contragewichtgewichten te berekenen
Hoe contragewichtgewichten te berekenen Wie heeft meer protonen neon of silicium?
Wie heeft meer protonen neon of silicium?  Hoe zijn ook grondwater en afvoer?
Hoe zijn ook grondwater en afvoer?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

