
Wetenschap
Hoeveel chlooratomen zijn er nodig om aan te sluiten met één calciumatoom?
* calcium (ca) is een metaal in groep 2 van de periodiek systeem, wat betekent dat het 2 valentie -elektronen heeft (elektronen in de buitenste schaal).
* chloor (Cl) is een niet -metaal in groep 17, wat betekent dat het 7 valentie -elektronen heeft en er nog een wil krijgen om zijn octet te voltooien.
Om stabiliteit te bereiken, verliest calcium zijn 2 valentie -elektronen en wordt hij een +2 kation (ca²⁺). Elk chlooratoom krijgt één elektron en wordt een -1 anion (CL⁻). Om de ladingen in evenwicht te brengen, hebt u twee chlooratomen nodig om de twee elektronen uit één calciumatoom te accepteren:
* ca²⁺ + 2cl⁻ → Cacl₂
Dit vormt het samengestelde calciumchloride (CACL₂).
 Is zout hetzelfde als natrium?
Is zout hetzelfde als natrium?  Hoe zou MG veranderen om nobele gasstructuur te krijgen?
Hoe zou MG veranderen om nobele gasstructuur te krijgen?  Wanneer materiaal opgelost en wordt gedragen in het geroepen water?
Wanneer materiaal opgelost en wordt gedragen in het geroepen water?  Waarom is het belangrijk dat Aufbau- en Lewis-diagrammen de nadruk lijken te leggen op elektronen?
Waarom is het belangrijk dat Aufbau- en Lewis-diagrammen de nadruk lijken te leggen op elektronen?  Onderzoekers ontdekken dat gel littekenweefsel vermindert na operatie bij dieren
Onderzoekers ontdekken dat gel littekenweefsel vermindert na operatie bij dieren
 Meer kinderen en jongeren verdrinken doordat de opwarming van de aarde onstabiel meerijs veroorzaakt
Meer kinderen en jongeren verdrinken doordat de opwarming van de aarde onstabiel meerijs veroorzaakt Wat is de aard van bezinning?
Wat is de aard van bezinning?  Wat orkanen betekenen voor Red Tide
Wat orkanen betekenen voor Red Tide Methoden om de risico's van smeltende gletsjers te verminderen
Methoden om de risico's van smeltende gletsjers te verminderen Studie daagt de evolutietheorie van vogels van dinosauriërs uit - was het andersom?
Studie daagt de evolutietheorie van vogels van dinosauriërs uit - was het andersom?
Hoofdlijnen
- Je bent niet wat je eet
- Welk organisme gebruiken wetenschappers om koolstofdioxide te eten?
- Wat is het maening van de ademhaling?
- Beweging van DNA gekoppeld aan de reactie op schade, het vermogen om zichzelf te herstellen
- Is uw hond agressief? Een dierenarts legt het woedesyndroom uit
- Hebben dierencellen en planten een celmembraan?
- Is ornithologie een tak van zoölogie?
- Komt de evolutie op het niveau van organismen op?
- In welke fase condenseren en verkorten de chromatinevezels in chromosomen die zichtbaar zijn onder microscoop?
- Chemici remmen een kritische versnelling van celonsterfelijkheid
- Kinderen houden niet van bloemkool, broccoli kan in hun microbioom worden geschreven

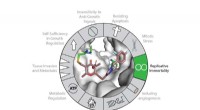
- Milieuvriendelijke productie van geneesmiddelen Nobelprijswinnaars meest trotse prestatie

- Het verwijderen van giftig kwik uit verontreinigd water

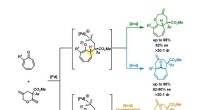
- Uiteenlopende synthese van bicyclische middelgrote ringstructuren
 Hoe verschilt een carbonylgroep van carboxylgroep?
Hoe verschilt een carbonylgroep van carboxylgroep?  Wat is de kleinste eenheid van een organisme dat een specifieke functie heeft?
Wat is de kleinste eenheid van een organisme dat een specifieke functie heeft?  Wanneer enzymen worden geplaatst in extreme pH- of temperatuuromstandigheden, ontspannen ze en veranderen van vorm, wat wordt dit genoemd?
Wanneer enzymen worden geplaatst in extreme pH- of temperatuuromstandigheden, ontspannen ze en veranderen van vorm, wat wordt dit genoemd?  Waterplanten met speciale adaptieve functies
Waterplanten met speciale adaptieve functies Oppervlakte van een driehoek met 10 voet basis en 8 hoogte?
Oppervlakte van een driehoek met 10 voet basis en 8 hoogte?  Elektronisch toezicht heeft de recidive van meisjes in het jeugdstrafrecht niet teruggedrongen, zegt studie
Elektronisch toezicht heeft de recidive van meisjes in het jeugdstrafrecht niet teruggedrongen, zegt studie Hoe oefenen de luchtdeeltjes druk uit op de binnenkant van de ballon?
Hoe oefenen de luchtdeeltjes druk uit op de binnenkant van de ballon?  Mannen zien voedsel minder snel als een kwestie van nationale veiligheid tijdens een pandemie
Mannen zien voedsel minder snel als een kwestie van nationale veiligheid tijdens een pandemie
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

