
Wetenschap
Wat gebeurt er als ijzer wordt ondergedompeld in kopersulfaatoplossing en waarom?
* IJzer wordt bedekt met koper: Je ziet een roodbruine coating die op het ijzer vormt. Dit komt omdat ijzer reactiever is dan koper.
* De blauwe kopersulfaatoplossing wordt bleek: De blauwe kleur van de kopersulfaatoplossing vervaagt terwijl de koperionen reageren met het ijzer.
* De oplossing kan enigszins groen worden: Dit komt door de vorming van ijzer (II) sulfaat, wat een lichtgroene oplossing is.
Dit is waarom dit gebeurt:
1. Verplaatsingsreactie: Dit is een klassiek voorbeeld van een verplaatsingsreactie. Een meer reactief metaal (ijzer) verplaatst een minder reactief metaal (koper) van zijn zoutoplossing.
2. Iron's reactiviteit: IJzer is hoger op de reactiviteitsreeks dan koper. Dit betekent dat het een sterkere neiging heeft om elektronen te verliezen en positieve ionen te vormen.
3. Reactievergelijking: De reactie kan worden weergegeven door de volgende vergelijking:
`` `
Fe (s) + CUSO₄ (aq) → feso₄ (aq) + cu (s)
`` `
* ijzer (Fe) reageert met kopersulfaat (cuso₄) .
* ijzer (ii) sulfaat (feso₄) wordt gevormd in oplossing.
* koper (cu) wordt afgezet op het ijzeroppervlak.
Samenvattend: Het ijzer verplaatst het koper van de kopersulfaatoplossing, vormt ijzer (II) sulfaat en veroorzaakt een roodbruine koperen coating op het ijzer.
 Terwijl Aziatische steden zinken, beheerde retraite moet worden ingediend
Terwijl Aziatische steden zinken, beheerde retraite moet worden ingediend Wat heeft deze spookachtige sporen in de lucht achtergelaten?
Wat heeft deze spookachtige sporen in de lucht achtergelaten?  Vergelijking van varens en bloeiende planten
Vergelijking van varens en bloeiende planten  Hoge niveaus van PFAS beïnvloeden het immuunsysteem, leverfuncties in gestreepte bas van Cape Fear River
Hoge niveaus van PFAS beïnvloeden het immuunsysteem, leverfuncties in gestreepte bas van Cape Fear River Hoe boomkrekels op elkaars liedjes afstemmen
Hoe boomkrekels op elkaars liedjes afstemmen
Hoofdlijnen
- Nieuw onderzoek onderzoekt hoe kankercellen zich in het menselijk lichaam verspreiden
- Hoe sneller ze komen:hoe de sociale status tussen vissen wordt onderhandeld
- Moleculaire simulaties verklaren hoe enzymatische pompen calciumionen in spiercellen transporteren
- Hoe schat ik de celgrootte met behulp van een microscoop?
- Hoe verschillen de vier soort DNA -nucleotiden van elkaar?
- Denk je dat je een hersenschudding hebt? Een bloedtest kan het diagnosticeren
- Waar worden eiwitten in alle cel gemaakt?
- Waarom definiëren wetenschappers systemen?
- Is de oorsprong van replicatie of vork hetzelfde?
- LED's maken de weg vrij voor betere medicamenteuze therapieën

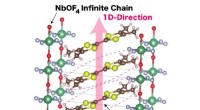
- Onderzoekers ontdekken nieuwe organische dirigent
- Laatste bevindingen over bittere stoffen in koffie
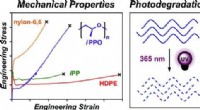
- Chemici maken sneller afbreekbaar plastic voor gebruik op zee
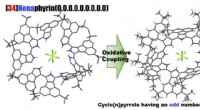
- Synthese van een bijna-infrarood lichtabsorberende macrocyclische aromatische verbinding
 Wat is gifgas?
Wat is gifgas?  Hoe op te lossen voor de eindtemperatuur in een calorimeter
Hoe op te lossen voor de eindtemperatuur in een calorimeter  Wat beweegt water tussen het aardoppervlak en de atmosfeer weer terug?
Wat beweegt water tussen het aardoppervlak en de atmosfeer weer terug?  Fiscale prikkels kunnen de CO2-uitstoot in ontwikkelingslanden helpen verminderen
Fiscale prikkels kunnen de CO2-uitstoot in ontwikkelingslanden helpen verminderen Kunnen bomen algenbloei tegengaan?
Kunnen bomen algenbloei tegengaan? Een atoom heeft 11 protonen 13 neutronen en elektronen Wat zijn mogelijk isotopen van dit atoom?
Een atoom heeft 11 protonen 13 neutronen en elektronen Wat zijn mogelijk isotopen van dit atoom?  De cycloonoverstromingen in Mozambique waren verwoestend voor dieren; we bestudeerden hoe de lichaamsgrootte de overleving beïnvloedde
De cycloonoverstromingen in Mozambique waren verwoestend voor dieren; we bestudeerden hoe de lichaamsgrootte de overleving beïnvloedde  Hoeveel ons in 1 keizerlijke ounce?
Hoeveel ons in 1 keizerlijke ounce?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

