
Wetenschap
Hoeveel gram stikstofdioxide moet reageren met water om 5,00 x 1022 moleculen monoxide te produceren?
1. Schrijf de gebalanceerde chemische vergelijking:
3 No₂ (G) + H₂o (L) → 2 Hno₃ (aq) + No (G)
2. Bepaal de molverhouding tussen stikstofdioxide (NO₂) en stikstofmonoxide (NO):
Uit de evenwichtige vergelijking zien we dat 3 mol No₂ reageert om 1 mol nr.
3. Converteer moleculen van NO naar mol:
* Avogadro's nummer:6.022 x 10²³ Moleculen/mol
* Mol No =(5,00 x 10²² moleculen) / (6.022 x 10²³ Moleculen / mol) =0,0830 mol Nr.
4. Bereken mol No₂ nodig:
* Mol No₂ =(0,0830 mol NO) * (3 mol No₂ / 1 mol No) =0,249 mol No₂
5. Converteer mol No₂ om te grammen:
* Molaire massa van No₂ =14,01 g/mol (n) + 2 * 16.00 g/mol (O) =46.01 g/mol
* Gram van no₂ =(0.249 mol No₂) * (46.01 g/mol) = 11,4 g no₂
Daarom moet 11,4 gram stikstofdioxide reageren met water om 5,00 x 10²² moleculen van stikstofmonoxide te produceren.
 Na een afwezigheid van tachtig jaar zijn grijze wolven teruggekeerd naar Colorado – hoe de herintroductie het ecosysteem zal beïnvloeden
Na een afwezigheid van tachtig jaar zijn grijze wolven teruggekeerd naar Colorado – hoe de herintroductie het ecosysteem zal beïnvloeden  Studie onderzoekt de gevolgen van toegenomen rook op Californische meren
Studie onderzoekt de gevolgen van toegenomen rook op Californische meren  Wereld wordt geconfronteerd met klimaatapartheid:VN-expert
Wereld wordt geconfronteerd met klimaatapartheid:VN-expert Hoe je kritisch kunt denken, kun je valse klimaatclaims opsporen
Hoe je kritisch kunt denken, kun je valse klimaatclaims opsporen  Wat is een voorbeeld van principe?
Wat is een voorbeeld van principe?
Hoofdlijnen
- Wat doen wetenschappers die puur onderzoek doen?
- Vergelijk ATP met een gevonden voorwerp in uw huishouden. Wat zijn de overeenkomsten en verschillen?
- Hoe evolueerden gewervelde dieren voor het eerst hun kaken?
- Hoe is een organisme voorbeeld van een systeem?
- Wat is een niet-epitheelcel?
- Wat is een vrijlevend organisme?
- Onderzoek roept op tot een herbestemming van inputsubsidies om duurzame IPM-praktijken te bevorderen
- Wat is een wetenschappelijk uitgangspunt?
- Kaperparasiet geblokkeerd voor infiltratie van bloed
- Verrassende ontdekking van spinnenhaar kan leiden tot sterkere lijmen
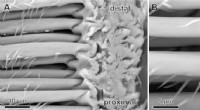
- Zelfherstellende levende materialen gebruikt als 3D-bouwstenen
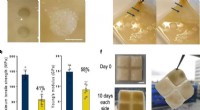
- Nieuwe aanpak creëert een uitzonderlijke katalysator met één atoom voor watersplitsing

- Nanocilindervibraties helpen bij het kwantificeren van polymeeruitharding voor 3D-printen
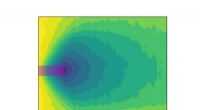
- Opslag van thermische energie:materiaal absorbeert warmte als het smelt en geeft het weer af als het stolt

 Een middelzwaar zwart gat verbergt zich in het midden van een gigantische sterrenhoop
Een middelzwaar zwart gat verbergt zich in het midden van een gigantische sterrenhoop Hoeveel groeiseizoenen overleven planten met kruidachtige meestal?
Hoeveel groeiseizoenen overleven planten met kruidachtige meestal?  Wat is dominante negatieve mutatie?
Wat is dominante negatieve mutatie?  Onderzoekers ontwikkelen een interventie die recidive vermindert bij kinderen die opnieuw naar school gaan vanuit het rechtssysteem
Onderzoekers ontwikkelen een interventie die recidive vermindert bij kinderen die opnieuw naar school gaan vanuit het rechtssysteem Heeft natrium een volledige buitenste valentie -schaal?
Heeft natrium een volledige buitenste valentie -schaal?  Wat is Mars Mineral Geology?
Wat is Mars Mineral Geology?  Burgerwetenschap:de ecologische voetafdruk van uw voedsel kennen
Burgerwetenschap:de ecologische voetafdruk van uw voedsel kennen Opruiming Fukushima vermindert stralingsniveaus, maar niet alles
Opruiming Fukushima vermindert stralingsniveaus, maar niet alles
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

