
Wetenschap
Schrijf evenwichtige moleculaire en netto ionische vergelijkingen voor de reacties van hydrobromzuur met magnesium?
reacties van hydrobromzuur met magnesium
Moleculaire vergelijking:
2 HBR (aq) + mg (s) → mgBr₂ (aq) + h₂ (g)
Netto ionische vergelijking:
2 H⁺ (aq) + mg (s) → mg²⁺ (aq) + h₂ (g)
Verklaring:
* Moleculaire vergelijking: Deze vergelijking toont de volledige chemische formules van alle reactanten en producten.
* Netto ionische vergelijking: Deze vergelijking toont alleen de soort die direct deelneemt aan de reactie. We laten toeschouwersionen weg, die ionen zijn die in dezelfde vorm aan beide zijden van de vergelijking bestaan. In dit geval is BR⁻ een toeschouwer -ion.
afbraak van de reactie:
* reactanten: Hydrobrominezuur (HBR) is een sterk zuur, wat betekent dat het volledig ioniseert in oplossing om H⁺- en Br⁻ -ionen te vormen. Magnesium (mg) is een vast metaal.
* Producten: Magnesiumbromide (MgBr₂) is een oplosbare ionische verbinding die zich in oplossing vormt. Waterstofgas (H₂) is een product van de reactie en wordt vrijgegeven als bubbels.
Sleutelpunten:
* Dit is een enkele verplaatsingsreactie, waarbij magnesium waterstof uit het zuur verplaatst.
* De reactie is exotherme, wat betekent dat het warmte vrijgeeft.
* Het geproduceerde waterstofgas is ontvlambaar, dus de reactie moet worden uitgevoerd in een goed geventileerd gebied.
 Heeft natriumchloride een hoger smelt- en kookpunt?
Heeft natriumchloride een hoger smelt- en kookpunt?  Welke heeft de lagere atoommassa kobalt of nikkel?
Welke heeft de lagere atoommassa kobalt of nikkel?  Onderzoekers creëren biomateriaal dat zowel een krachtig medicijn als gendempers levert
Onderzoekers creëren biomateriaal dat zowel een krachtig medicijn als gendempers levert Waarom zou je aandacht besteden aan de fysieke toestanden van alle reactanten en producten bij het schrijven van evenwichtsconstante-uitdrukkingen?
Waarom zou je aandacht besteden aan de fysieke toestanden van alle reactanten en producten bij het schrijven van evenwichtsconstante-uitdrukkingen?  Welk punt op een fasediagram vertegenwoordigt smeltpunt?
Welk punt op een fasediagram vertegenwoordigt smeltpunt?
 Sterke aardbeving schudt Perus hoofdstad Lima
Sterke aardbeving schudt Perus hoofdstad Lima De Mekongdelta in Vietnam zinkt. Kan sediment het redden?
De Mekongdelta in Vietnam zinkt. Kan sediment het redden? Wat is ecologische realiteiten in de Filippijnse Contex?
Wat is ecologische realiteiten in de Filippijnse Contex?  Wetenschappers creëren grootste verzameling koraalrifkaarten ooit gemaakt
Wetenschappers creëren grootste verzameling koraalrifkaarten ooit gemaakt In de wetenschap een uitspraak over hoe dingen in de natuur werken?
In de wetenschap een uitspraak over hoe dingen in de natuur werken?
Hoofdlijnen
- Onderzoekers ontsluiten het mysterie van hoe ‘handigheid’ ontstaat
- Moleculaire simulaties verklaren hoe enzymatische pompen calciumionen in spiercellen transporteren
- Het oversteken van organismen van de F1 -generatie produceert welke generatie?
- Geheugen, depressie, slapeloosheid - en wormen?
- Wat is wetenschappelijke notatie voor 420?
- Wat is de basiseenheid van DNA waar het van heeft gemaakt?
- Hoe dieren getallen begrijpen, beïnvloedt hun overlevingskansen
- Waarin wordt massa gelabeld?
- Wat zijn een organismen die met elkaar en hun omgeving omgaan?
- Energiezuinige groene route naar magnesiumproductie

- Video:Lifehacks voor scheikunde:voedseleditie

- Volledig inkjet-geprinte op vanadiumdioxide gebaseerde radiofrequentieschakelaars voor flexibele herconfigureerbare componenten

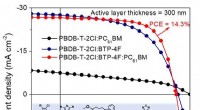
- Meer dan 14% efficiëntie voor ternaire organische zonnecel met 300 nm dikke actieve laag
- Nieuwe interactie tussen dunne-filmmagneten voor snellere geheugenapparaten

 Monsterbeeld van de Fornax Galaxy Cluster
Monsterbeeld van de Fornax Galaxy Cluster Hoe zit het met bladverliezende bomen in de winter is niet waar?
Hoe zit het met bladverliezende bomen in de winter is niet waar?  Wat is eerlijk wild op volle zee?
Wat is eerlijk wild op volle zee?  Battle Epic:Wanneer orkanen botsen met vulkanen
Battle Epic:Wanneer orkanen botsen met vulkanen  Polymethacrylzuur-methylacrylaat-copolymeer msds?
Polymethacrylzuur-methylacrylaat-copolymeer msds?  Wanneer is incompatibiliteit fysiek van aard?
Wanneer is incompatibiliteit fysiek van aard?  Studie benadrukt de menselijke maat van een warmer klimaat
Studie benadrukt de menselijke maat van een warmer klimaat Wat gebeurt er met de fasegrens van water bij 1 atm?
Wat gebeurt er met de fasegrens van water bij 1 atm?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

