
Wetenschap
Hoe kan een absorptiespectrum een samenstelling identificeren?
Hier is een uitsplitsing van hoe het werkt:
1. energieniveaus: Atomen en moleculen hebben specifieke, gekwantiseerde energieniveaus die elektronen kunnen bezetten. Deze energieniveaus zijn uniek voor elk element en molecuul.
2. absorptie: Wanneer het licht op een stof schijnt, kunnen de fotonen in het licht elektronen in de atomen of moleculen van de stof opwinden. Als de energie van het foton overeenkomt met het energieverschil tussen twee energieniveaus in de stof, absorbeert het elektron het foton en springt het naar een hoger energieniveau.
3. Specifieke golflengten: Elk element en molecuul absorberen fotonen van specifieke golflengten, overeenkomend met de energieverschillen tussen de elektronenergieniveaus. Deze absorptie resulteert in "donkere lijnen" of "absorptiebanden" in het spectrum van licht dat door de stof is gegaan.
4. Unieke vingerafdruk: Het patroon van geabsorbeerde golflengten (het absorptiespectrum) is uniek voor elk element en molecuul. Dit unieke patroon werkt als een "vingerafdruk" waarmee wetenschappers de samenstelling van een stof kunnen identificeren.
Voorbeeld:
* waterstof: Waterstofatomen hebben een specifiek absorptiespectrum met een sterke lijn bij 656,3 nm (rood), een andere bij 486,1 nm (blauwgroen) en andere in het ultraviolette bereik. Als u deze lijnen in een onbekend monster observeert, kunt u met vol vertrouwen waterstof identificeren als een component.
* organische moleculen: Organische moleculen hebben complexe absorptiespectra vanwege de aanwezigheid van verschillende functionele groepen (zoals C =O, C-H, enz.). Deze groepen absorberen specifieke golflengten in de ultraviolette, zichtbare en infraroodgebieden en helpen onderzoekers de structuur van het molecuul te identificeren.
Toepassingen:
* Astronomie: Absorptiespectra worden gebruikt om elementen en moleculen te identificeren die aanwezig zijn in sterren, planeten en andere hemellichamen.
* chemie: Absorptiespectroscopie wordt veel gebruikt in analytische chemie om onbekende stoffen te identificeren, hun concentratie te kwantificeren en hun chemische reacties te bestuderen.
* Biologie: Absorptiespectroscopie speelt een cruciale rol bij het bestuderen van biomoleculen zoals eiwitten en DNA, waardoor informatie wordt geboden over hun structuur en functie.
Beperkingen:
* Gevoeligheid: De gevoeligheid van absorptiespectroscopie kan worden beperkt door de concentratie van de analyt en de sterkte van de absorptie.
* Interferentie: Andere stoffen in het monster kunnen ook licht absorberen, waardoor de analyse van de doelverbinding mogelijk wordt verstoord.
Over het algemeen is absorptiespectroscopie een krachtig hulpmiddel voor het identificeren en analyseren van de samenstelling van materie. Door de relatie tussen energieniveaus, absorptie en specifieke golflengten te begrijpen, kunnen we de unieke vingerafdrukken van absorptiespectra gebruiken om waardevolle inzichten in de wereld om ons heen te krijgen.
 Welke voordelen heeft water als een universeel oplosmiddel?
Welke voordelen heeft water als een universeel oplosmiddel?  Wanneer natrium reageert met chloor wint of verliest het een elektron?
Wanneer natrium reageert met chloor wint of verliest het een elektron?  Het bouwen van Europese steden met hout zou de helft van de huidige koolstofemissies van de cementindustrie vastleggen en opslaan
Het bouwen van Europese steden met hout zou de helft van de huidige koolstofemissies van de cementindustrie vastleggen en opslaan Nieuwe methode om adsorbentia te recyclen bij de behandeling van afvalwater
Nieuwe methode om adsorbentia te recyclen bij de behandeling van afvalwater  Chemici volgen hoe medicijnen veranderen en het griepvirus blokkeren
Chemici volgen hoe medicijnen veranderen en het griepvirus blokkeren
 Moeder weet het het beste:hoe planten hun nakomelingen helpen door seizoensaanwijzingen door te geven
Moeder weet het het beste:hoe planten hun nakomelingen helpen door seizoensaanwijzingen door te geven  Nieuw onderzoek laat zien hoe bomen de lucht in Londen reinigen
Nieuw onderzoek laat zien hoe bomen de lucht in Londen reinigen  Waarom nemen consumenten deel aan 'groene' programma's?
Waarom nemen consumenten deel aan 'groene' programma's?  Het Silverback Gorilla's Dieet
Het Silverback Gorilla's Dieet  Tropische bosbranden in Colombia pieken na vredesakkoorden van 2016
Tropische bosbranden in Colombia pieken na vredesakkoorden van 2016
Hoofdlijnen
- Hoe zit het met sommige bacteriën is belangrijk voor mensen in termen van het feit dat we in staat zijn om maker -eiwitten en nucleïnezuren te zijn van het voedsel dat je eet?
- Heeft nucleaire deling plaatsgevonden in mitose of intrphase?
- Welk cijfer zou het meest nuttig zijn voor het tonen van complexe processen zoals celdeling?
- Tagged slakken om onderzoekers te helpen de groei van de slakkenpopulatie te volgen
- Mammoetprojecten om Noorse viskwekerijen milieuvriendelijk te maken
- Inzicht in hoe cellen reageren op fysieke signalen zou tot nieuwe ziektebehandelingen kunnen leiden
- Uit onderzoek blijkt dat de afkoeling van de oceaan gedurende millennia heeft geleid tot grotere vissen
- Wat kunnen genetici over genen leren door RNA te bestuderen?
- Waarom worden cellen de basiseenheid van het leven genoemd?
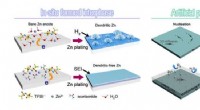
- Interfaciale chemie verbetert de oplaadbaarheid van Zn-batterijen
- Polymere membranen gebruiken om industriële scheidingen op te ruimen

- Legeronderzoekers doen explosieve ontdekking

- Focus op de zuurstofreductiereactie bij het zoeken naar efficiëntere waterstofcellen

- Wetenschappers bij ESS, Zweeds wateronderzoek, ORNL gebruikt VISION om te kijken naar veelvoorkomende verontreinigingen voor toepassingen in schoner water

 NASA krijgt een laatste blik op tropische depressie Enawos laatste buiging
NASA krijgt een laatste blik op tropische depressie Enawos laatste buiging Hoe beïnvloedt zure regen gebouwen en standbeelden?
Hoe beïnvloedt zure regen gebouwen en standbeelden?  Redenen achter gamerwoede bij kinderen zijn complex en kinderen zijn goed in het benoemen ervan
Redenen achter gamerwoede bij kinderen zijn complex en kinderen zijn goed in het benoemen ervan Wat zijn de harde en snelle wetenschapsregels. Zijn er?
Wat zijn de harde en snelle wetenschapsregels. Zijn er?  Is de staart van een komeet gecreëerd door verwarmde zon?
Is de staart van een komeet gecreëerd door verwarmde zon?  Het effect van zonlicht op dieren en planten
Het effect van zonlicht op dieren en planten Belangrijke keuzes van universiteiten kunnen loonverschillen tussen mannen en vrouwen voorspellen
Belangrijke keuzes van universiteiten kunnen loonverschillen tussen mannen en vrouwen voorspellen NASA bereidt zich voor op lancering Parker Solar Probe, een missie om de zon aan te raken
NASA bereidt zich voor op lancering Parker Solar Probe, een missie om de zon aan te raken
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

