
Wetenschap
Welke voordelen heeft water als een universeel oplosmiddel?
1. Polariteit en waterstofbinding:
* polariteit: Watermoleculen zijn polair, wat betekent dat ze een enigszins positief uiteinde hebben (waterstofatomen) en een enigszins negatief uiteinde (zuurstofatoom). Met deze polariteit kan water andere polaire moleculen en ionen aantrekken en interageren, waardoor ze effectief uit elkaar worden getrokken en oplost.
* waterstofbinding: De waterstofatomen in watermoleculen kunnen waterstofbruggen vormen met andere polaire moleculen, waardoor het oplossend vermogen verder wordt verbeterd. Deze sterke interacties verstoren de bindingen die de opgeloste stof bij elkaar houden, wat leidt tot ontbinding.
2. Hoge diëlektrische constante:
* Water heeft een hoge diëlektrische constante, wat betekent dat het effectief de elektrostatische krachten tussen ionen in een oplossing verzwakt. Dit verzwakt de aantrekkingskracht tussen tegengesteld geladen ionen, waardoor het voor hen gemakkelijker wordt om te scheiden en op te lossen.
3. Overvloed en toegankelijkheid:
* Water is ongelooflijk overvloedig op aarde, waardoor het direct beschikbaar is voor het oplossen van stoffen. De toegankelijkheid ervan speelt een belangrijke rol in het belang ervan als oplosmiddel voor verschillende processen.
4. Biologische betekenis:
* De oplosbare eigenschappen van het water zijn cruciaal voor het leven. Het werkt als een oplosmiddel voor voedingsstoffen, zuurstof en andere essentiële moleculen in biologische systemen. Het vergemakkelijkt chemische reacties en transporteert stoffen binnen organismen.
5. Veelzijdigheid:
* Water kan een breed scala aan stoffen oplossen, waaronder zouten, suikers, zuren en sommige gassen. Deze veelzijdigheid maakt het een essentieel onderdeel in verschillende industriële en binnenlandse toepassingen.
Het is echter belangrijk om te onthouden dat water niet echt een universeel oplosmiddel is:
* Hoewel water veel stoffen oplost, lost het niet alles op. Vetten en oliën zijn bijvoorbeeld niet-polair en zijn meestal onoplosbaar in water.
* De oplosbaarheid van een stof in water hangt af van factoren zoals temperatuur, druk en de aard van de opgeloste stof.
Ondanks deze beperkingen hebben de uitzonderlijke oplossingsmogelijkheden van het water het onmisbaar gemaakt in verschillende aspecten van ons leven, van biologische processen tot industriële toepassingen.
 Welke van de volgende is niet gebonden aan het centrale koolstofatoom in een aminozuur?
Welke van de volgende is niet gebonden aan het centrale koolstofatoom in een aminozuur?  Hoe de atoomstructuur van atomen
Hoe de atoomstructuur van atomen Chemische octopus vangt stiekeme aanwijzingen voor kanker, sporen van glycoproteïnen
Chemische octopus vangt stiekeme aanwijzingen voor kanker, sporen van glycoproteïnen Gericht op ijzeropname om een nieuwe klasse antibiotica tegen urineweginfecties te creëren
Gericht op ijzeropname om een nieuwe klasse antibiotica tegen urineweginfecties te creëren Wat is de heldere gele vloeistof die wordt gezien na een gevormde stolsel?
Wat is de heldere gele vloeistof die wordt gezien na een gevormde stolsel?
 Warmste september van afgelopen maand wereldwijd gemeten:EU
Warmste september van afgelopen maand wereldwijd gemeten:EU Wat de tanden van wolven onthullen over hun leven
Wat de tanden van wolven onthullen over hun leven  Vijf manieren waarop kunst kan helpen de plasticcrisis op te lossen
Vijf manieren waarop kunst kan helpen de plasticcrisis op te lossen Wat zijn de verschillende belangrijke rollen die u kunt spelen om onze natuurlijke hulpbronnen te behouden?
Wat zijn de verschillende belangrijke rollen die u kunt spelen om onze natuurlijke hulpbronnen te behouden?  Tunesië pionier in mediterrane zeewierteelt
Tunesië pionier in mediterrane zeewierteelt
Hoofdlijnen
- Nieuw onderzoek laat zien hoe de malariaparasiet groeit en zich vermenigvuldigt
- Welk type wetenschapper past het beste bij het gebied dat zij zouden bestuderen?
- Wat zijn de eindproducten van glycolyse naast ATP?
- Roze + roze =goud? De veren van hybride kolibries komen niet overeen met die van zijn ouders
- Wat is iets dat dezelfde functie vervult als nucleolus in de cel?
- Doodt zuiveringszout kankercellen in het menselijk lichaam?
- Hoe helpt marihuana de gezondheid van mensen
- Onderzoekers ontdekken wat pneumokokken je ziek maken
- Welke bijdrage heeft Carl Linnaeus geleverd aan de evolutie?
- Molecuul uit de natuur zorgt voor volledig recyclebare polymeren

- Eenden bieden onderzoekers een unieke kans om menselijke aanraking te bestuderen
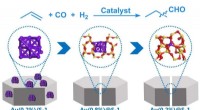
- Onderzoekers ontwikkelen nieuwe Au-katalysator voor hydroformylering
- Cysteïnesynthese was een belangrijke stap in het ontstaan van leven:studie

- Wetenschappers brengen voor het eerst belangrijk immuunsysteem-enzym in kaart
 Wat doen homologe chromosomen in profase 1?
Wat doen homologe chromosomen in profase 1?  "What Are Oxidants?
"What Are Oxidants? Is er een oceaan onder onze voeten?
Is er een oceaan onder onze voeten?  Wat zijn de 7 diatomische elementen?
Wat zijn de 7 diatomische elementen? Een samengestelde machine maken voor een schoolproject
Een samengestelde machine maken voor een schoolproject  Sommige componenten van inkt worden minimaal aangetrokken tot de stationaire fase en zeer oplosbaar in oplosmiddel waar deze zich op filterpapier bevinden tijdens chromatografie?
Sommige componenten van inkt worden minimaal aangetrokken tot de stationaire fase en zeer oplosbaar in oplosmiddel waar deze zich op filterpapier bevinden tijdens chromatografie?  Kleine halfgeleidende kristallen zijn veelbelovend voor zonnecelarchitecturen en lichtgevende apparaten
Kleine halfgeleidende kristallen zijn veelbelovend voor zonnecelarchitecturen en lichtgevende apparaten  Verre 'ruimtesneeuwman' ontsluit mysterie over hoe sommige slapende objecten in de diepe ruimte 'ijsbommen' worden
Verre 'ruimtesneeuwman' ontsluit mysterie over hoe sommige slapende objecten in de diepe ruimte 'ijsbommen' worden
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

