
Wetenschap
Waarom zijn metalen betere geleiders dan keramiek?
metalen:
* gratis elektronen: Metalen hebben een "zee" van gedelokaliseerde elektronen die niet strak gebonden zijn aan een bepaald atoom. Deze elektronen zijn vrij om door het materiaal te bewegen, waardoor het gemakkelijk transport van elektrische lading mogelijk is.
* Metallic binding: De atomen in metalen worden bij elkaar gehouden door een "zee" van gedelokaliseerde elektronen, die bijdragen aan hun hoge geleidbaarheid.
* Hoge elektronenmobiliteit: De vrije elektronen in metalen kunnen snel en gemakkelijk bewegen in reactie op een elektrisch veld, waardoor ze uitstekende geleiders van elektriciteit en warmte zijn.
keramiek:
* Covalente binding: Keramiek wordt meestal bij elkaar gehouden door sterke covalente bindingen, waarbij elektronen worden gedeeld tussen atomen. Deze bindingen zijn gelokaliseerd, wat betekent dat de elektronen niet vrij zijn om gemakkelijk te bewegen.
* ionische binding: Sommige keramiek heeft ook ionische bindingen, waarbij elektronen worden overgebracht tussen atomen, waardoor geladen ionen ontstaan. Dit kan de elektronenmobiliteit verder beperken.
* Beperkte elektronenmobiliteit: De sterke en gelokaliseerde binding in keramiek beperkt de beweging van elektronen, wat leidt tot slechte geleidbaarheid.
Samenvattend:
Metalen hebben vrij bewegende elektronen vanwege hun bindingstructuur, waardoor ze uitstekende geleiders zijn. Keramiek, met hun sterke en gelokaliseerde binding, heeft een beperkte elektronenmobiliteit, wat resulteert in een slechte geleidbaarheid.
Hoofdlijnen
- Een nieuw hoofdstuk in de druiventeelt:niet-transgene plantenregeneratietechnologie
- Wanneer een groep cellen die allemaal dezelfde basisstructuur en functie hebben samenkomen, wat vormen ze dan?
- Is intelligentie een genetisch kenmerk?
- Waarom kan een cel veel rRNA maken, maar slechts één kopie van het DNA?
- Eiwitsynthese in eukaryoten en prokaryoten?
- Wat zijn de twee soorten observatie in de wetenschappelijke methode?
- Welk lichaamssysteem beschermt de terugbereiken buitenlandse stoffen?
- Hoe een onderzoeker meet variabele onderzoeksvariabele is wat?
- Baanbrekende veldproeven tonen het potentieel van genbewerking in gewassen aan
- Plastic afval omzetten in waterstofgas en koolstofnanobuisjes

- Hoe bacteriën mangaanoxide nanodeeltjes produceren

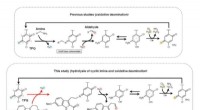
- Onderzoekers kijken naar de natuur om de geheimen van cyclische imine-splitsing te ontrafelen
- Snel 3D-printen met zichtbaar licht

- Het voordeel van 2D metaal-organische raamwerk nanosheets in detectietoepassingen

 Mondiale oceaanstromingen verklaren waarom het noordelijk halfrond drassiger is
Mondiale oceaanstromingen verklaren waarom het noordelijk halfrond drassiger is  Welke bloedgroep is altijd heterozygoot?
Welke bloedgroep is altijd heterozygoot?  Waarom zou een oude hoofdreeksster meer helium hebben?
Waarom zou een oude hoofdreeksster meer helium hebben?  Wat zijn voorbeelden van vaste en gasmengsels?
Wat zijn voorbeelden van vaste en gasmengsels?  Video:Matthias Maurer:training voor een ruimtewandeling
Video:Matthias Maurer:training voor een ruimtewandeling Atmosferische breking maakt de daglichturen een beetje wat?
Atmosferische breking maakt de daglichturen een beetje wat?  Hoe maak je een aardappelklok?
Hoe maak je een aardappelklok?  Ingenieurs bestuderen zwevende vleermuizen en kolibries in Costa Rica
Ingenieurs bestuderen zwevende vleermuizen en kolibries in Costa Rica
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com


