
Wetenschap
Hoe vind je het theoretische kookpunt van een oplossing?
1. Begrijp het concept van kookpunthoogte:
* Puur oplosmiddel: Een puur oplosmiddel heeft een specifiek kookpunt.
* Oplossing: Wanneer een opgeloste stof (zoals zout) wordt opgelost in een oplosmiddel (zoals water), neemt het kookpunt van de oplossing toe. Dit fenomeen wordt kookpunthoogte genoemd.
2. Gebruik de formule:
De formule voor het berekenen van het kookpunthoogte is:
Δtb =kb * m
Waar:
* Δtb: De verandering in kookpunt (in ° C of ° F)
* KB: Het molale kookpunthoogte -constante (een eigenschap van het oplosmiddel, in ° C/molaal of ° F/molaal)
* m: De molaliteit van de oplossing (mol opgeloste stof per kilogram oplosmiddel)
3. Bereken de molaliteit (M):
* molaliteit: Molaliteit (M) is het aantal mol opgeloste opgeloste opgeloste mol in 1 kg oplosmiddel.
* om m: te vinden
* Bepaal de mol opgeloste stof.
* Bepaal de massa van het oplosmiddel in kg.
* Verdeel de mol opgeloste stof door de massa van het oplosmiddel in kg.
4. Zoek het molaal kookpunthoogte -hoogteconstante (KB) op:
* KB is een specifieke eigenschap van het oplosmiddel. U kunt het vinden in tabellen of referentiematerialen.
* Bijvoorbeeld:
* KB voor water is 0,512 ° C/molaal.
* KB voor benzeen is 2,53 ° C/molaal.
5. Bereken de verandering in kookpunt (Δtb):
* Sluit de waarden voor KB en M aan op de formule.
* Bereken Δtb.
6. Bepaal het theoretische kookpunt:
* Voeg de verandering in kookpunt (Δtb) toe aan het normale kookpunt van het zuivere oplosmiddel.
Voorbeeld:
Wat is het theoretische kookpunt van een oplossing die 0,5 mol NaCl bevat opgelost in 1 kg water?
* kb voor water =0,512 ° C/molaal
* m =0,5 mol / 1 kg =0,5 molaal
* Δtb =kb * m =0,512 ° C/molaal * 0,5 molaal =0,256 ° C
* Normaal kookpunt van water =100 ° C
* Theoretisch kookpunt van de oplossing =100 ° C + 0,256 ° C =100.256 ° C
belangrijke opmerkingen:
* De formule veronderstelt ideale oplossingen, waarbij de interacties tussen opgeloste stof en oplosmiddel minimaal zijn.
* De formule is voor niet-vluchtige opgeloste stoffen. Voor vluchtige opgeloste stoffen moet u rekening houden met de dampdruk van de opgeloste stof.
* De hoogte van het kookpunt is een colligatieve eigenschap, wat betekent dat het afhangt van de concentratie van opgeloste deeltjes, niet op hun identiteit.
 Afstudeerder vindt dat het toevoegen van verse koolstof aan permafrost koolstofverlies veroorzaakt
Afstudeerder vindt dat het toevoegen van verse koolstof aan permafrost koolstofverlies veroorzaakt Voedselketen met drie organismen die Humans
Voedselketen met drie organismen die Humans NASA kijkt naar hardnekkige overblijfselen van ex-tropische cycloon Iris
NASA kijkt naar hardnekkige overblijfselen van ex-tropische cycloon Iris De antropogene toename van koolstofdioxide op aarde is ongekend
De antropogene toename van koolstofdioxide op aarde is ongekend Wetenschappers schatten de ijsdikte en subglaciale terreinen in de Yulong-sneeuwberg
Wetenschappers schatten de ijsdikte en subglaciale terreinen in de Yulong-sneeuwberg
Hoofdlijnen
- Waarom tapdansen vervende gifkikkers?
- Welke van de volgende technologieën opende een nieuwe takwetenschap in de jaren 1970 A. Lichtmicroscoop B. Veranderende genen Bacteriën C. Centrifuge D. Chromatografie?
- Wat is basofiele degeneratie?
- Wat is een voorbeeld van kern?
- 5 stadia van mitose
- Waar in de cel vindt u nucleïnezuren?
- Wat betekent het plant verspreiding?
- GMO-experimenten
- De uitgebreide kreten om voedsel van zangvogels vertonen de eerste tekenen van stemonderwijs
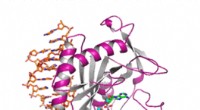
- Wetenschappers ontcijferen de structuur, belangrijkste kenmerken van een essentieel immuunsurveillance-eiwit bij mensen
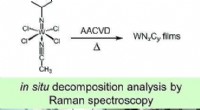
- Gesimuleerde chemische dampafzetting van een wolfraamcarbonitride-precursor
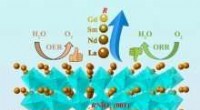
- Afstemming van de elektrokatalytische prestaties van bifunctionele katalysatoren
- 3D-printen verandert nanomachines in levensgrote arbeiders

- Diagnostische vooruitgang:gasgevoelige capsule komt in 2022 op de markt

 Afbeelding:Stervorming in de Chamaeleon
Afbeelding:Stervorming in de Chamaeleon Een licht schijnen op moleculen:L-vormige metamaterialen kunnen de lichtrichting regelen
Een licht schijnen op moleculen:L-vormige metamaterialen kunnen de lichtrichting regelen  Hoe equivalente uitdrukkingen te vinden
Hoe equivalente uitdrukkingen te vinden Hoe verschillende overtuigingen en attitudes de loopbaanambities van studenten beïnvloeden
Hoe verschillende overtuigingen en attitudes de loopbaanambities van studenten beïnvloeden  Zijn er meer eencellige of meercellige organismen op aarde?
Zijn er meer eencellige of meercellige organismen op aarde?  Hoe B te vinden in Y = Mx + B
Hoe B te vinden in Y = Mx + B  De voordelen en nadelen van niet-hernieuwbare energiebronnen
De voordelen en nadelen van niet-hernieuwbare energiebronnen Touchscreens gaan 3D met knoppen die pulseren en trillen onder je vingertoppen
Touchscreens gaan 3D met knoppen die pulseren en trillen onder je vingertoppen
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

