
Wetenschap
Wat is de eigenschappen van zout?
eigenschappen van zout (natriumchloride, NaCl)
Zout of natriumchloride (NaCl) is een veel voorkomende verbinding met veel interessante eigenschappen:
Fysieke eigenschappen:
* uiterlijk: Wit, kristallijne vaste stof
* smaak: Zout
* Oplosbaarheid: Zeer oplosbaar in water, enigszins oplosbaar in alcohol
* smeltpunt: 801 ° C (1474 ° F)
* kookpunt: 1465 ° C (2669 ° F)
* Dichtheid: 2.16 g/cm³
* Hardheid: 2.5 op de Mohs Hardness Scale
* kristallijne structuur: Kubiek
chemische eigenschappen:
* ionische verbinding: Samengesteld uit positief geladen natriumionen (Na+) en negatief geladen chloride-ionen (CL-) samengehouden door elektrostatische aantrekkingskracht.
* Neutrale pH: Zoutoplossingen hebben een neutrale pH van 7, wat betekent dat ze noch zuur noch basic zijn.
* elektrolyt: Leidt elektriciteit wanneer opgelost in water.
* reageert met zuren: Zout reageert met zuren om een nieuw zout en een nieuw zuur te vormen. Natriumchloride reageert bijvoorbeeld met zwavelzuur om natriumsulfaat en zoutzuur te vormen.
* reageert met bases: Zout reageert met bases om een nieuw zout en een nieuwe basis te vormen. Natriumchloride reageert bijvoorbeeld met natriumhydroxide om natriumhydroxide en natriumchloride te vormen.
Andere opmerkelijke eigenschappen:
* conserveermiddel: Zout wordt gebruikt om voedsel te behouden door microbiële groei te remmen.
* smaakverbeteraar: Zout is essentieel voor de menselijke gezondheid en voegt smaak toe aan voedsel.
* de-ibing agent: Zout verlaagt het vriespunt van water en wordt gebruikt om ijs te smelten op wegen en trottoirs.
* Industrieel gebruik: Zout wordt gebruikt in verschillende industriële processen, waaronder de productie van chloor, natriumhydroxide en andere chemicaliën.
Opmerking: Deze eigenschappen zijn voor puur natriumchloride. De eigenschappen van tafelzout, waaronder additieven zoals jodium, kunnen enigszins variëren.
 Welke verbinding wordt gevormd met chloor en zink?
Welke verbinding wordt gevormd met chloor en zink?  Is er een onvertankelijk alkaan dat 49 waterstofatomen bevat?
Is er een onvertankelijk alkaan dat 49 waterstofatomen bevat?  Wat is het verschil tussen vrij chloor en totaal chloor?
Wat is het verschil tussen vrij chloor en totaal chloor?  Uit welke elementen bestaat C6H1306?
Uit welke elementen bestaat C6H1306?  Hoe noemt u een oplossing waarin de maximale hoeveelheid oplosmiddel is opgelost, nog meer opgeloste opgeloste stof, zal als kristallen op de onderste container zitten?
Hoe noemt u een oplossing waarin de maximale hoeveelheid oplosmiddel is opgelost, nog meer opgeloste opgeloste stof, zal als kristallen op de onderste container zitten?
 Hoe mannelijke libellen de vleugelkleur aanpassen aan de temperatuur
Hoe mannelijke libellen de vleugelkleur aanpassen aan de temperatuur  Littekens achtergelaten door Australische onderzeese aardverschuivingen onthullen toekomstig tsunami-potentieel
Littekens achtergelaten door Australische onderzeese aardverschuivingen onthullen toekomstig tsunami-potentieel Wetenschappers onderzoeken verband tussen zoutgehalte van oppervlaktewater, klimaatverandering
Wetenschappers onderzoeken verband tussen zoutgehalte van oppervlaktewater, klimaatverandering Microben kunnen optreden als poortwachters van Earths Deep Carbon
Microben kunnen optreden als poortwachters van Earths Deep Carbon Amerikaanse leraar roeit solo in recordtijd over Atlantische Oceaan
Amerikaanse leraar roeit solo in recordtijd over Atlantische Oceaan
Hoofdlijnen
- Welke aanpassingen heeft een zegel?
- Wat is een fokexperiment dat ouders in één personage anders gebruikt?
- Moeten we ons zorgen maken dat onze katten en honden COVID krijgen?
- Zijn mensen het slimste dier?
- Wat veroorzaakt de beweging van voedsel door dikke darm?
- Hoe een haai te volgen:Nieuw onderzoek onthult waar, waarom en hoe haaienvissen elkaar overlappen
- Welk kenmerk van het levende organisme amoebe of paramecium en spirogyra?
- Welke van de divisies vaatplanten heeft meer leden?
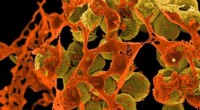
- Wetenschappers ontdekken hoe sommige bacteriën antibiotica overleven
- Systematische studie lost discussie over katalysatorontwerp voor uitlaatgassen van auto's op

- Wetenschappers ontdekken een nieuwe manier om resistente bacteriën aan te pakken
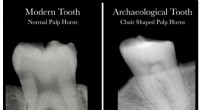
- Wetenschap ontmoet archeologie met ontdekking dat tandheelkundige röntgenfoto's vitamine D-tekort onthullen
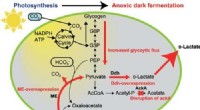
- Methode levert een hoog percentage D-lactaat op met behulp van cyanobacteriën, kan een revolutie teweegbrengen in de productie van bioplastic
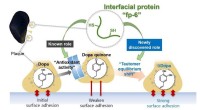
- Hoe mosselen hun hechting onder water behouden
 Heeft Buzz Aldrin vóór de vlucht in de ruimte gevlogen toen hij op de maan landde?
Heeft Buzz Aldrin vóór de vlucht in de ruimte gevlogen toen hij op de maan landde?  Negatieve exponenten: regels voor vermenigvuldigen en delen
Negatieve exponenten: regels voor vermenigvuldigen en delen  Welke 2 eigenschappen worden gebruikt om luchtmassa's gekarakteriseerd te worden?
Welke 2 eigenschappen worden gebruikt om luchtmassa's gekarakteriseerd te worden?  theoretisch, numerieke studie van grafeenplaten onthult eigenschappen die kunnen leiden tot nieuwe opto-elektrische apparaten
theoretisch, numerieke studie van grafeenplaten onthult eigenschappen die kunnen leiden tot nieuwe opto-elektrische apparaten Hoe het massamiddelpunt
Hoe het massamiddelpunt Wat is jouw idee om 3D-printen op de maan - om het als thuis te laten voelen?
Wat is jouw idee om 3D-printen op de maan - om het als thuis te laten voelen? Democratieën die meer geneigd zijn om oorlogen te beginnen, behalve wanneer dat niet het geval is
Democratieën die meer geneigd zijn om oorlogen te beginnen, behalve wanneer dat niet het geval is Naar welk type cel behoort een ribosoom?
Naar welk type cel behoort een ribosoom?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

