
Wetenschap
Wat voor soort binding is het wanneer suiker oplost in water?
* Suiker (sucrose) Structuur: Suikermoleculen hebben veel hydroxylgroepen (-oH) die polair zijn.
* Polariteit van het water: Watermoleculen zijn ook polair vanwege het elektronegativiteitsverschil tussen zuurstof- en waterstofatomen, wat resulteert in een gedeeltelijke negatieve lading op zuurstof en gedeeltelijke positieve ladingen op hydrogenen.
* waterstofbinding: De gedeeltelijk positieve waterstofatomen van watermoleculen kunnen zwakke elektrostatische attracties (waterstofbruggen) vormen met de gedeeltelijk negatieve zuurstofatomen van de hydroxylgroepen in suiker.
Het proces:
1. Hydratatie: Watermoleculen omringen de suikermoleculen.
2. Waterstofbinding: De waterstofbindingen tussen water- en suikermoleculen verstoren de intermoleculaire krachten die de suikermoleculen in het kristalrooster vasthouden.
3. Oplossing: De suikermoleculen worden gescheiden en verspreid over het water en vormen een oplossing.
Sleutelpunten:
* Terwijl waterstofbinding de primaire kracht is, van der Waals Forces Draag ook bij aan de interactie tussen water- en suikermoleculen.
* Het oplossingsproces is omkeerbaar . Als u de oplossing verwarmt, zullen de watermoleculen meer kinetische energie hebben, de waterstofbruggen breken en de suiker zal opnieuw kristalliseren.
Laat het me weten als je op een van deze punten meer details wilt!
 Hoe komt het materiaal van de grond en lucht naar dieren?
Hoe komt het materiaal van de grond en lucht naar dieren?  Bonenboomplan om Amazon te beschermen
Bonenboomplan om Amazon te beschermen Wolven in een vliegtuig:hoe het opvangcentrum erin slaagde vier ernstig bedreigde pups opnieuw te verwilderen
Wolven in een vliegtuig:hoe het opvangcentrum erin slaagde vier ernstig bedreigde pups opnieuw te verwilderen  Waarom droogte-veroorzakende regen afhankelijk is van de tropische oceanen
Waarom droogte-veroorzakende regen afhankelijk is van de tropische oceanen  Onderzoeksvliegtuig op grote hoogte verkent de bovenste niveaus van de Aziatische moesson
Onderzoeksvliegtuig op grote hoogte verkent de bovenste niveaus van de Aziatische moesson
Hoofdlijnen
- Het wordt het interne proces genoemd dat voedsel absorbeerbaar maakt?
- Hebben octopussen, inktvissen en krabben emoties?
- Wat is de vorm van cellen gevonden in stengels?
- Turkije bevrijdt 7, 500 illegaal opgejaagde kikkers de rivier in
- Studie onthult hoe cellen de groei van hun structurele filamenten organiseren
- Welk weefsel vormt de aveoli?
- Wat betekent GI in de biologie?
- Luipaarden doden minstens 3 kinderen op het Indiase platteland
- Hoe microben in ‘startculturen’ gefermenteerde worst lekker maken
- Polymere membranen gebruiken om industriële scheidingen op te ruimen

- Nanocoating maakt lichtgewicht metaalschuim bothard en explosieveilig

- Binnenkort:een bloedtest voor de ziekte van Alzheimer?

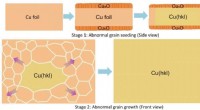
- Het afstemmen van het oppervlak geeft variaties op metaalfolies
- Machine learning-software voorspelt gedrag van bacteriën
 Nucleaire diagnostiek helpt de weg vrij te maken voor ontsteking op NIF-traagheidsopsluitingsfusie
Nucleaire diagnostiek helpt de weg vrij te maken voor ontsteking op NIF-traagheidsopsluitingsfusie Studie brengt nieuwe klimaatmodellen van kleine ster TRAPPIST 1s zeven intrigerende werelden
Studie brengt nieuwe klimaatmodellen van kleine ster TRAPPIST 1s zeven intrigerende werelden Hightech borderwandplan te zien op CES
Hightech borderwandplan te zien op CES Hoe worden planeten geboren?
Hoe worden planeten geboren?  Hoe snel moet een object gaan om de zwaartekracht van planeten te verlaten?
Hoe snel moet een object gaan om de zwaartekracht van planeten te verlaten?  Wanneer een astronaut op de maan landt, wat is zijn massa?
Wanneer een astronaut op de maan landt, wat is zijn massa?  Orkaan Iota scheurt door Midden-Amerika na aanlanding Nicaragua
Orkaan Iota scheurt door Midden-Amerika na aanlanding Nicaragua Waarom zingen mensen onder de douche?
Waarom zingen mensen onder de douche?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

