
Wetenschap
Gebruik de deeltjestheorie van materie om uit te leggen waarom tafelzout sneller oplost dan rotszout?
De deeltjestheorie van materie
* materie is gemaakt van deeltjes: Alle stoffen zijn samengesteld uit kleine deeltjes die constant bewegen.
* deeltjes hebben spaties tussen hen: Er is ruimte tussen de deeltjes, waardoor beweging en interactie mogelijk is.
* Deeltjes zijn in constante beweging: De deeltjes trillen altijd en beweegt zich rond. Deze beweging neemt toe met temperatuur.
* De sterkte van aantrekkingskracht tussen deeltjes beïnvloedt de toestand van materie: Sterkere attracties leiden tot vaste stoffen, zwakkere aantrekkingskracht op vloeistoffen en zeer zwakke attracties op gassen.
De theorie toepassen op zoutoplossing
1. Oppervlakte: Tafelzout heeft een veel groter oppervlak dan gesteentezout vanwege de kleinere deeltjesgrootte. Dit betekent dat meer deeltjes tafelzout op elk moment aan het water worden blootgesteld.
2. Deeltjesbeweging: De kleinere deeltjes tafelzout hebben meer oppervlakte en worden gemakkelijker verplaatst door de watermoleculen. Deze watermoleculen kunnen gemakkelijker interageren met de zoutdeeltjes en breken de ionische bindingen die de zoutkristallen bij elkaar houden.
3. Snelheid van oplossing: Het verhoogde oppervlak en een efficiëntere beweging van de kleinere deeltjes van tafelzout zorgen voor een groter aantal zoutdeeltjes om in het water met een snellere snelheid op te lossen.
Samenvattend:
* De deeltjestheorie van materie verklaart dat kleinere deeltjes meer oppervlakte hebben, wat leidt tot frequentere botsingen en interacties met de watermoleculen.
* Door deze verhoogde interactie kunnen de watermoleculen de zoutkristallen effectiever breken, wat leidt tot snellere oplossing.
* Daarom lost tafelzout, met zijn kleinere deeltjesgrootte, sneller op dan rotszout.
 Macromolecuul voornamelijk gemaakt van koolstof- en waterstofatomen?
Macromolecuul voornamelijk gemaakt van koolstof- en waterstofatomen?  Geleiden covalente verbindingen elektriciteit als vloeistof of als vaste stof?
Geleiden covalente verbindingen elektriciteit als vloeistof of als vaste stof?  Waarom zijn basebrandwonden erger dan zuurbrandwonden?
Waarom zijn basebrandwonden erger dan zuurbrandwonden?  Hoeveel zink zat er in het carbonaat?
Hoeveel zink zat er in het carbonaat?  Hoe verhouden de eigenschappen van nieuwe stoffen zich tot oude stoffen?
Hoe verhouden de eigenschappen van nieuwe stoffen zich tot oude stoffen?
 Nieuw internationaal initiatief benadrukt de noodzaak van wereldwijde actie tegen luchtvervuiling, aangezien de gevolgen voor de gezondheid groot blijven
Nieuw internationaal initiatief benadrukt de noodzaak van wereldwijde actie tegen luchtvervuiling, aangezien de gevolgen voor de gezondheid groot blijven Aangespoord door egels:hoe zeelelies hun opstaan kregen
Aangespoord door egels:hoe zeelelies hun opstaan kregen  NASA's meerdere weergaven van orkaan Dorian vanuit de ruimte
NASA's meerdere weergaven van orkaan Dorian vanuit de ruimte Samengestelde gevaren vormen een verhoogd risico voor dichtbevolkte regio's in de Himalaya
Samengestelde gevaren vormen een verhoogd risico voor dichtbevolkte regio's in de Himalaya 'Tijd om te eten':Video's laten zien dat het tikken van de tenen door kikkers een strategie kan zijn om prooien uit te lokken
'Tijd om te eten':Video's laten zien dat het tikken van de tenen door kikkers een strategie kan zijn om prooien uit te lokken
Hoofdlijnen
- Wat is DNA in de mitochondria?
- Wat is het verschil tussen draagvermogen en biotisch potentieel?
- Onderzoekers gebruiken het ritme van DNA-replicatie om kankercellen te doden
- Functies van menselijke organen
- Polygene eigenschappen: definitie, voorbeeld en feiten
- Wat is het samenvoegen van een mannelijke reproductieve cel met vrouwelijke cel?
- Wat zijn vier voorbeelden van imperfecte schimmel?
- Wat zijn de sterke punten van de biogenesetheorie?
- Hoe het epigenetische landschap de binding van pioniertranscriptiefactoren moduleert
- Pandemie biedt unieke kans voor atmosferische chemici

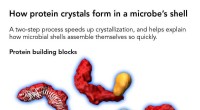
- Wetenschappers ontdekken hoe eiwitten kristallen vormen die een microbenomhulsel betegelen
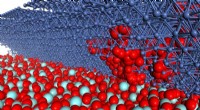
- Atomair nauwkeurige modellen verbeteren het begrip van brandstofcellen
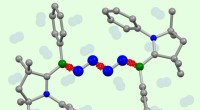
- Inerte stikstof gedwongen om met zichzelf te reageren
- Een nieuwe manier om moleculen te maken voor de ontwikkeling van geneesmiddelen

 Welke chemische stof vormt calciumoxide als het aan water wordt toegevoegd?
Welke chemische stof vormt calciumoxide als het aan water wordt toegevoegd?  Wat is de kleur van de zon?
Wat is de kleur van de zon?  Wat zijn alle onderdelen in een dierencel genoemd?
Wat zijn alle onderdelen in een dierencel genoemd?  Magnetar-mysteries in onze melkweg en daarbuiten
Magnetar-mysteries in onze melkweg en daarbuiten Wat zou een voorbeeld zijn van een wetenschappelijke theorie?
Wat zou een voorbeeld zijn van een wetenschappelijke theorie?  SpaceX Starship landt rechtop, explodeert dan in de laatste test
SpaceX Starship landt rechtop, explodeert dan in de laatste test Richtlijnen voor de industrie prijzen niet-geteste technologie als klimaatoplossing
Richtlijnen voor de industrie prijzen niet-geteste technologie als klimaatoplossing Wetenschappers brengen nieuwe inzichten in de erfelijkheid van de ernst van de hiv-infectie
Wetenschappers brengen nieuwe inzichten in de erfelijkheid van de ernst van de hiv-infectie
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

