
Wetenschap
Wat zijn de belangrijkste ideeën in de kerntheorie van Atom?
1. Atomen zijn samengesteld uit een kleine, dichte, positief geladen kern omgeven door negatief geladen elektronen.
* Nucleus: Deze centrale regio bevat bijna alle massa van het atoom. Het bestaat uit protonen (positief geladen deeltjes) en neutronen (Neutrale deeltjes).
* elektronen: Deze deeltjes zijn veel kleiner dan protonen en neutronen en rond de kern in een wolkachtige structuur.
2. Het atoom is meestal lege ruimte.
* De kern is ongelooflijk klein in vergelijking met de totale grootte van het atoom. Dit betekent dat het grootste deel van het atoom daadwerkelijk lege ruimte is.
3. Het aantal protonen in de kern bepaalt het element.
* Dit wordt het atoomnummer genoemd . Alle koolstofatomen hebben bijvoorbeeld 6 protonen, alle zuurstofatomen hebben 8 protonen, enzovoort.
4. Het aantal neutronen in de kern kan variëren, waardoor isotopen ontstaan.
* isotopen zijn atomen van hetzelfde element met verschillende aantallen neutronen. Carbon-12 en koolstof-14 zijn bijvoorbeeld beide isotopen van koolstof, maar koolstof-12 heeft 6 neutronen terwijl koolstof-14 8 neutronen heeft.
5. Elektronen bezetten specifieke energieniveaus of schalen rond de kern.
* Deze energieniveaus zijn gekwantiseerd, wat betekent dat elektronen alleen kunnen bestaan in discrete energietoestanden. Hoe verder een elektron uit de kern komt, hoe hoger zijn energieniveau.
6. Chemische reacties omvatten de interacties van elektronen in de buitenste schaal van atomen.
* De opstelling van elektronen in deze energieniveaus bepaalt hoe atomen met elkaar omgaan en chemische bindingen vormen.
Belangrijke bijdragen aan de nucleaire theorie:
* Ernest Rutherford: Zijn beroemde Gold Foil Experiment (1911) leverde het eerste bewijs op voor een kleine, dichte, positief geladen kern.
* niels bohr: Zijn model van het atoom (1913) beschreef elektronen die de kern ronddraaien in gekwantiseerde energieniveaus.
* James Chadwick: Zijn ontdekking van het neutron in 1932 voltooide ons begrip van de kern.
Dit zijn de belangrijkste ideeën in de nucleaire theorie van het atoom. Het is belangrijk om te onthouden dat dit model een vereenvoudigde weergave van het atoom is, en er zijn nog steeds veel dingen die we niet weten over de structuur en het gedrag ervan.
 Waarom vormen alleen de elementen in HOFBrINCl covalente bindingen?
Waarom vormen alleen de elementen in HOFBrINCl covalente bindingen?  Welke elementen op het periodiek systeem zijn puur?
Welke elementen op het periodiek systeem zijn puur?  Zonnemateriaal voor het produceren van schone waterstofbrandstof
Zonnemateriaal voor het produceren van schone waterstofbrandstof Wat is de chemische reactie tussen een alkali of base en een zuur?
Wat is de chemische reactie tussen een alkali of base en een zuur?  Wat kan er gebeuren met het kookpunt van inhoud als er onzuiverheden aanwezig zijn?
Wat kan er gebeuren met het kookpunt van inhoud als er onzuiverheden aanwezig zijn?
 Meer voorkomen, minder ophalen. Toenemende plasticvervuiling leidt tot verandering in aanpak
Meer voorkomen, minder ophalen. Toenemende plasticvervuiling leidt tot verandering in aanpak Het pad naar onze evolutie
Het pad naar onze evolutie Welke dieren eten eendekroos?
Welke dieren eten eendekroos?  Waarom stoppen bij plastic zakken en rietjes? Het pleidooi voor een wereldwijd verdrag dat de meeste plastics voor eenmalig gebruik verbiedt
Waarom stoppen bij plastic zakken en rietjes? Het pleidooi voor een wereldwijd verdrag dat de meeste plastics voor eenmalig gebruik verbiedt Welke aanpassingen hebben omnivoren om te overleven in het gematigde bos?
Welke aanpassingen hebben omnivoren om te overleven in het gematigde bos?
Hoofdlijnen
- Noem drie delen die elke cel heeft?
- Hoe zijn computervirussen vergelijkbaar met en verschillend van biologische virussen?
- Welk deel van de plant produceert zaden?
- Welk enzym is betrokken bij RNA -verlenging?
- Waarom is meiose belangrijk in een organisme?
- Wetenschappers ontdekken dat schorpioenen zich richten op hun gif
- Welke cellen kunnen niet delen na de geboorte bij mensen?
- Inzicht in het mechanisme van schade door ultraviolet licht en kankerlaesies kan bijdragen aan antikankertherapie
- Welke kenmerken hebben alle prokaryoten gemeen?
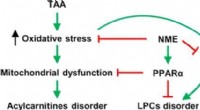
- Verborgen kracht van nootmuskaat:de lever helpen
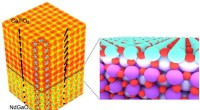
- Een 3D-beeldvormingstechniek ontgrendelt eigenschappen van perovskietkristallen
- Oppervlakken die als gekkovoeten vastgrijpen, kunnen gemakkelijk in massa worden geproduceerd

- Nieuwe methode om het duurzaamheidsprobleem van plastic op te lossen

- Doorbraak in de medicamenteuze chemie kan leiden tot betere geneesmiddelen

 Het primaire filter om eiwitten uit te sluiten van het filtraat is de?
Het primaire filter om eiwitten uit te sluiten van het filtraat is de?  Waar kan wetenschap voor worden gebruikt?
Waar kan wetenschap voor worden gebruikt?  Gemodelleerde wolken in de tropen krijgen een reality check
Gemodelleerde wolken in de tropen krijgen een reality check 100 gram is hetzelfde als 10 kg?
100 gram is hetzelfde als 10 kg?  Hoe Liquid Propaan naar gas om te zetten
Hoe Liquid Propaan naar gas om te zetten  Wat is onderlinge afhankelijkheid van planten en mensen?
Wat is onderlinge afhankelijkheid van planten en mensen?  Wat te verwachten van Disney+ streamingdienst:Ja, het bevat Marvel en Star Wars
Wat te verwachten van Disney+ streamingdienst:Ja, het bevat Marvel en Star Wars Waarom flikkeren sterren rood in de nachtelijke hemel?
Waarom flikkeren sterren rood in de nachtelijke hemel?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

