
Wetenschap
Is deze vergelijking evenwichtig en in de laagste vorm 4NH3-2N2 6H2?
Dit is waarom:
* stikstof (n): Aan de linkerkant heb je 1 stikstofatoom in NH3 (en omdat er 4 NH3 -moleculen zijn, zijn het 4 stikstofatomen in totaal). Aan de rechterkant heb je 2 stikstofatomen in N2.
* waterstof (h): Aan de linkerkant heb je 3 waterstofatomen in NH3 (en 12 in totaal omdat er 4 NH3 zijn). Aan de rechterkant heb je 6 waterstofatomen in H2.
Hier is de evenwichtige vergelijking:
2 NH3 → N2 + 3 H2
Verklaring:
* stikstof: Om de stikstof in evenwicht te brengen, plaatsen we een coëfficiënt van 2 voor NH3 aan de linkerkant.
* waterstof: Dit balanceert automatisch de waterstof, omdat er nu 6 waterstofatomen aan beide zijden zijn.
Deze evenwichtige vergelijking toont aan dat 2 moleculen ammoniak (NH3) ontleden om 1 molecuul stikstofgas (N2) en 3 moleculen waterstofgas (H2) te vormen.
 Lichtgewicht van periodiek systeem speelt grote rol in het leven op aarde
Lichtgewicht van periodiek systeem speelt grote rol in het leven op aarde Switch-in-a-cell elektriseert het leven
Switch-in-a-cell elektriseert het leven Het atoom aantal koolstof is 6. Give Two Pieces Information die dit je geeft over het atoom?
Het atoom aantal koolstof is 6. Give Two Pieces Information die dit je geeft over het atoom?  Zijn binaire moleculaire verbindingen gemaakt van twee kationen?
Zijn binaire moleculaire verbindingen gemaakt van twee kationen?  Wat is de edelgasnotatie voor cesium?
Wat is de edelgasnotatie voor cesium?
 Wetenschappers geven eerste gedetailleerde schattingen van hoeveel sediment vanuit het rifsysteem naar koraaleilanden wordt aangevoerd
Wetenschappers geven eerste gedetailleerde schattingen van hoeveel sediment vanuit het rifsysteem naar koraaleilanden wordt aangevoerd  Wat zijn twee manieren waarop wetenschappers de geschiedenis van de aardklimaten kunnen bestuderen?
Wat zijn twee manieren waarop wetenschappers de geschiedenis van de aardklimaten kunnen bestuderen?  Wat zou het belang kunnen zijn van culturele ecosysteemdiensten op zee en aan de kust?
Wat zou het belang kunnen zijn van culturele ecosysteemdiensten op zee en aan de kust? Dollars en geuren:hoe de juiste geuren het winkelend publiek kunnen aanmoedigen om gezonder voedsel te kopen
Dollars en geuren:hoe de juiste geuren het winkelend publiek kunnen aanmoedigen om gezonder voedsel te kopen  Nieuwe analyse suggereert manieren voor landeigenaren om fracking en delfstofwinning zonder regelgeving te beperken
Nieuwe analyse suggereert manieren voor landeigenaren om fracking en delfstofwinning zonder regelgeving te beperken
Hoofdlijnen
- Paren uracil altijd met cytosine in het RNA -molecuul?
- Welk lichaamsdeel is verbonden met de keelholte?
- Waarom leven mannen niet zo lang als vrouwen?
- Artikel geeft een gedetailleerd overzicht van deelnemers aan Golden Retriever Lifetime Study
- Cellen geprogrammeerd als computers om ziekten te bestrijden
- Wat houdt ons tegen om algen en anaërobe bacteriën naar Mars te lanceren om te beginnen met terravorming voor mogelijke toekomstige bewoning?
- Wat is het voordeel van aseksuele sporen?
- Mycoheterotrofe planten als sleutel tot het Wood Wide Web
- Nieuwe hypothese:waarom bacteriën steeds resistenter worden tegen antibiotica
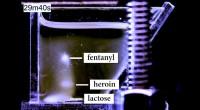
- Whisky verifiëren met laserlicht

- Nieuwe technologie kan wetshandhavers helpen kleinere hoeveelheden fentanyl met een hogere mate van nauwkeurigheid te detecteren
- Kan een hightech snuffelaar ons helpen beschermen?

- Werkende eiwitten maken goed gebruik van frustratie
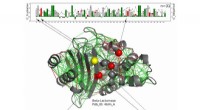
- Hoe de eerste biomoleculen gevormd konden zijn

 Ongekende 3D-beelden van levende cellen plus details van moleculen erin
Ongekende 3D-beelden van levende cellen plus details van moleculen erin Wat zijn de voor- en nadelen van het produceren van elektriciteit door foto -elektrische cellen?
Wat zijn de voor- en nadelen van het produceren van elektriciteit door foto -elektrische cellen?  Hoe een hekel aan lessen het vreemdgaan van studenten beïnvloedt
Hoe een hekel aan lessen het vreemdgaan van studenten beïnvloedt Hoe verhoudt de drijvende kracht op een volledig ondergedompeld object zich tot het gewicht van het verplaatste water?
Hoe verhoudt de drijvende kracht op een volledig ondergedompeld object zich tot het gewicht van het verplaatste water?  Wat is de maat voor hoeveel een straallicht dat buigt wanneer het materiaal binnenkomt?
Wat is de maat voor hoeveel een straallicht dat buigt wanneer het materiaal binnenkomt?  Welke informatie bewaart u in een zonboek?
Welke informatie bewaart u in een zonboek?  Emissiedoelen:Als er een (politieke) wil is, er is een manier
Emissiedoelen:Als er een (politieke) wil is, er is een manier Hoe zijn samengestelde ongelijkheden nuttig in het leven?
Hoe zijn samengestelde ongelijkheden nuttig in het leven?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

