
Wetenschap
Verdampt water een voorbeeld van oxidatie en waarom?
* oxidatie is een chemisch proces waarbij een stof elektronen verliest. Dit omvat vaak de toevoeging van zuurstof, maar niet altijd.
* verdamping is een fysiek proces waarbij een vloeistof verandert in een gas als gevolg van een toename van de temperatuur. Het omvat het verbreken van waterstofbruggen tussen watermoleculen, maar niet het verlies of winst van elektronen.
Hier is een uitsplitsing:
* water (h₂o) is een stabiel molecuul met twee waterstofatomen gebonden aan één zuurstofatoom. Het verkrijgt of verliest niet gemakkelijk elektronen in het verdampingsproces.
* verdamping omvat de watermoleculen die voldoende energie krijgen om de aantrekkelijke krachten te overwinnen die ze bij elkaar houden in de vloeibare toestand. Ze ontsnappen in de lucht als waterdamp.
Daarentegen is hier een voorbeeld van oxidatie:
* roesten van ijzer: IJzer (Fe) reageert met zuurstof (O₂) in aanwezigheid van vocht om ijzeroxide (Fe₂o₃) te vormen, beter bekend als roest. Deze reactie omvat het verlies van elektronen uit ijzeratomen, waardoor het een voorbeeld is van oxidatie.
Hoewel verdamping een verandering in de toestand van materie inhoudt, gaat het daarom niet in op het verlies van elektronen en is het dus niet een voorbeeld van oxidatie.
 Nieuwe test vindt nieuw mechanisme dat ten grondslag ligt aan veroudering van rode bloedcellen
Nieuwe test vindt nieuw mechanisme dat ten grondslag ligt aan veroudering van rode bloedcellen Wat zijn twee soorten stoffen mengen om emulsies te vormen?
Wat zijn twee soorten stoffen mengen om emulsies te vormen?  Wat is de procentuele opbrengst aan koolstofdisulfide als bij de reactie 33,4 g zwaveldioxide 10,1 g disulfide produceert?
Wat is de procentuele opbrengst aan koolstofdisulfide als bij de reactie 33,4 g zwaveldioxide 10,1 g disulfide produceert?  Wat is de formule en de naam van een hydrate bariumchloridewater?
Wat is de formule en de naam van een hydrate bariumchloridewater?  Regeling in de tijd van chemische reacties met alleen hoorbaar geluid
Regeling in de tijd van chemische reacties met alleen hoorbaar geluid
 Voor altijd chemicaliën in herten, jagers op vissen, toerisme
Voor altijd chemicaliën in herten, jagers op vissen, toerisme Aardbeving in Japan veroorzaakt kleine tsunami, 16 pijn
Aardbeving in Japan veroorzaakt kleine tsunami, 16 pijn Wat is de algemene betekenis voor de wetenschap?
Wat is de algemene betekenis voor de wetenschap?  Mensen zijn bereid meer te betalen om Everglades te beschermen als ze deze twee dingen weten
Mensen zijn bereid meer te betalen om Everglades te beschermen als ze deze twee dingen weten Wat voor soort plantenleven heeft Montana?
Wat voor soort plantenleven heeft Montana?
Hoofdlijnen
- Waarom classificeerden wetenschappers protisten terwijl er maar twee koninkrijken waren?
- Waarom wordt penicillium geclassificeerd als deuteromycota?
- Een grote stap in de richting van het verminderen van streptokokken bij op de boerderij gekweekte tilapia
- Wat gebeurt er als dieren geïsoleerd evolueren?
- De biodiversiteit van de aarde verandert naarmate de planeet opwarmt. Maar hoe?
- Is cultuur of cognitie werkelijk verantwoordelijk voor de taalstructuur?
- Hoe sociale dynamiek de darmmicroben van wilde maki's beïnvloedt
- Welke regels moet je volgen als wetenschapper?
- Wat gebeurt er met stikstof in een plant?
- Gefermenteerde zuivelproducten beter laten smaken

- Afbreekbare op suiker gebaseerde polymeren kunnen nuttige moleculaire vracht opslaan en vrijgeven

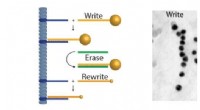
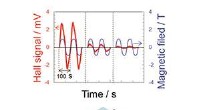
- Wetenschappers ontwikkelen lijm met industriële sterkte die kan worden losgemaakt in een magnetisch veld

- DNA als supramoleculaire bouwsteen
- Dageraad van organische eenkristalelektronica
 Wetenschappers synthetiseren 3D-grafeenfilms met hoogenergetische E-straal
Wetenschappers synthetiseren 3D-grafeenfilms met hoogenergetische E-straal Interactie tussen land en atmosfeer en kenmerken van wolkenneerslag op het Tibetaanse plateau
Interactie tussen land en atmosfeer en kenmerken van wolkenneerslag op het Tibetaanse plateau Wat is de chemische reactie die zink met salpeterzuur shwos om een (II) nitraatoplossing en waterstof te produceren?
Wat is de chemische reactie die zink met salpeterzuur shwos om een (II) nitraatoplossing en waterstof te produceren?  Wie heeft de computer uitgevonden?
Wie heeft de computer uitgevonden?  Kleine gouden sondes geven wetenschappers een idee van hoe ziekten zich ontwikkelen
Kleine gouden sondes geven wetenschappers een idee van hoe ziekten zich ontwikkelen  Insecteneiwit heeft een groot potentieel om de ecologische voetafdruk van Europese consumenten te verkleinen
Insecteneiwit heeft een groot potentieel om de ecologische voetafdruk van Europese consumenten te verkleinen Hoe de metrische voorvoegsels onthouden
Hoe de metrische voorvoegsels onthouden  Chemici vinden granaatscherven in de lucht
Chemici vinden granaatscherven in de lucht
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

