
Wetenschap
Wanneer zout op ijs wordt geplaatst, de smelt. Leg uit waarom?
1. Bevriezende puntdepressie
* Puur water bevriest bij 0 graden Celsius (32 graden Fahrenheit).
* zout (natriumchloride) lost op in water, waardoor een oplossing ontstaat.
* oplossingen hebben een lager vriespunt dan zuiver water. Dit wordt de depressie van het vriespunt genoemd.
2. Hoe zout ijs beïnvloedt
* zout lost op in de dunne laag water die zich van nature vormt op het ijsoppervlak.
* Dit oplossend proces absorbeert warmte uit de omgeving, inclusief het ijs zelf.
* Het ijs verliest warmte, waardoor de temperatuur onder zijn normale vriespunt daalt.
* Om een nieuw evenwicht te bereiken, smelt het ijs om deel uit te maken van de zoutwateroplossing.
3. Het effect van concentratie
* hoe meer zout u toevoegt, hoe lager het vriespunt van de oplossing.
* Dit is de reden waarom rotszout (die meestal natriumchloride is) effectiever is bij smeltend ijs dan tafelzout. Rotszout heeft een hogere concentratie natriumchloride.
4. Belangrijke opmerking:
* Zout smelt alleen ijs dat zich al op of onder het vriespunt bevindt. Als het ijs al boven het vriespunt staat, heeft zout geen effect.
Samenvattend verlaagt zout het vriespunt van water, waardoor ijs smelt omdat het warmte absorbeert en de temperatuur onder zijn vriespunt brengt.
 Wat zijn de 10 voorbeelden van wetenschappelijke houding?
Wat zijn de 10 voorbeelden van wetenschappelijke houding?  Waar het begint:jonge hongerige sprinkhanen stapelen zich op in Somalië
Waar het begint:jonge hongerige sprinkhanen stapelen zich op in Somalië Pacifics Palau dwingt toeristen om eco-belofte te ondertekenen
Pacifics Palau dwingt toeristen om eco-belofte te ondertekenen Bosbranden Australië laten drie doden minstens 150 huizen verloren
Bosbranden Australië laten drie doden minstens 150 huizen verloren Verlies van Arctisch zee-ijs kan Californië uitdrogen
Verlies van Arctisch zee-ijs kan Californië uitdrogen
Hoofdlijnen
- Waarom heeft de mens cultuur?
- Wat is fenpptype?
- Welk deel van de plant laat voedselwater en zuurstof door?
- Paradigmaverandering in de celbiologie? Eiwittransport blijkt niet te werken zoals we dachten
- Waar staat aminozuur voor?
- Waarom heeft de hartcel meer DNA?
- Hebben mitochondriën en chloroplasten ribosomen die vergelijkbaar zijn met structuur met die van bacteriën?
- Hoe worden veel orgelsystemen samengewerkt?
- De aanwijzing zit in de lijm:onderzoek laat zien hoe planten het bij elkaar houden tijdens de groei
- Aan koude aangepaste enzymen kunnen bij kamertemperatuur transformeren

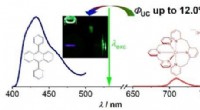
- Een nieuw pad voor duurzame opconversie van fotonen met niet-edele metalen
- Ingenieurs 3D-print vormveranderende slimme gel

- Waarom uien ons aan het huilen maken (en waarom sommigen niet)

- Water speelt een onverwachte rol bij de vorming van mineralen
 Anatomie van de ligamenten in de onderarmen
Anatomie van de ligamenten in de onderarmen Wanneer meer pijn meer winst betekent?
Wanneer meer pijn meer winst betekent? Luchtvervuiling sluit alle scholen in Teheran
Luchtvervuiling sluit alle scholen in Teheran Oorsprong en verspreiding van Euraziatische vruchten terug te voeren op de oude Zijderoute
Oorsprong en verspreiding van Euraziatische vruchten terug te voeren op de oude Zijderoute Hebben nobele gassen een volledig octet van elektronen?
Hebben nobele gassen een volledig octet van elektronen?  Sneeuwballenkans op aarde en vroege tekenen van leven
Sneeuwballenkans op aarde en vroege tekenen van leven Waarom lijkt de maan groter dan planeten en sterren?
Waarom lijkt de maan groter dan planeten en sterren?  Kleine aminozuurverschillen kunnen leiden tot dramatisch verschillende enzymen
Kleine aminozuurverschillen kunnen leiden tot dramatisch verschillende enzymen
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

