
Wetenschap
Hebben nobele gassen een volledig octet van elektronen?
Dit is waarom:
* octetregel: De octetregel stelt dat atomen de neiging hebben om elektronen te winnen, verliezen of delen om een stabiele configuratie van acht elektronen in hun buitenste energieniveau (valentie -schaal) te bereiken.
* Nobele gasconfiguratie: Nobele gassen hebben al acht elektronen in hun valentieschaal (behalve voor helium dat er twee heeft). Dit maakt ze zeer stabiel en niet -reactief, omdat ze niet nodig zijn om elektronen te winnen, te verliezen of te delen.
Voorbeeld:
* neon (ne): Heeft 10 elektronen, met de configuratie 2, 8 (twee in de eerste shell en acht in de tweede schaal). Dit is een volledig octet.
* helium (HE): Heeft 2 elektronen, met de configuratie 2. Dit is een volledig duet, dat de stabiele configuratie is voor het eerste energieniveau.
Vanwege hun stabiele elektronenconfiguraties worden edelgassen vaak "inerte gassen" genoemd. Het is echter belangrijk op te merken dat sommige edelgassen kunnen deelnemen aan chemische reacties onder specifieke omstandigheden.
 De scheikundige laat zien dat intermoleculaire interacties voorheen onbekende dimensies kunnen bereiken
De scheikundige laat zien dat intermoleculaire interacties voorheen onbekende dimensies kunnen bereiken Hoe de 'petro' uit de petrochemische industrie kan worden gehaald
Hoe de 'petro' uit de petrochemische industrie kan worden gehaald  Een beschrijving voor de formule H2O is twee?
Een beschrijving voor de formule H2O is twee?  Welke gassen in de lucht veroorzaken zure regen?
Welke gassen in de lucht veroorzaken zure regen?  Verborgen oorzaak van lage energie-efficiëntie van lithiumrijke kathodematerialen onthuld
Verborgen oorzaak van lage energie-efficiëntie van lithiumrijke kathodematerialen onthuld
 Het effect van temperatuur op de ademhaling van erwten
Het effect van temperatuur op de ademhaling van erwten  10, 000 geëvacueerd bij overstromingen in Canada terwijl reddingswerkers zoeken naar huisdieren
10, 000 geëvacueerd bij overstromingen in Canada terwijl reddingswerkers zoeken naar huisdieren Hoe het ontsluiten van de kracht van de natuur het VK kan helpen de strijd tegen klimaatverandering op te voeren
Hoe het ontsluiten van de kracht van de natuur het VK kan helpen de strijd tegen klimaatverandering op te voeren Klimaatprojecties laten zien dat er binnen dertig jaar gevolgen voor de menselijke gezondheid kunnen zijn
Klimaatprojecties laten zien dat er binnen dertig jaar gevolgen voor de menselijke gezondheid kunnen zijn  Biologisch of lokaal? Wat houdt de consument bezig als het gaat om produceren?
Biologisch of lokaal? Wat houdt de consument bezig als het gaat om produceren?
Hoofdlijnen
- Wat is dycenterie?
- Wanneer treedt melkzuurfermentatie op?
- Waarom wordt er meer ATP gegenereerd uit glucose in aanwezigheid van zuurstof?
- Meelkracht om voedselzekerheid te vergroten
- Research Paper Onderwerpen in Biochemistry
- Wat is de evolutie van primaten?
- Wat is DNA -splitsing?
- Wat is het huidige zeven stappensysteem om alle levende organismen te classificeren?
- Wordt de aanwezigheid van endomysium resulterend in skeletspiercellen die elektrisch van elkaar worden geïsoleerd?
- E-waste-etend eiwit creëert zeldzame aardelementen

- Onderzoekers ontsluiten een nieuwe methode voor het testen van op eiwit gebaseerde medicijnen
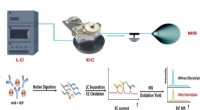
- Een mijlpaal in ultrasnelle gelfabricage van onconventionele zelfherstellende edelmetaalgels

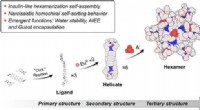
- Hexamere lanthanide-organische capsules met tertiaire structuur, opkomende functies
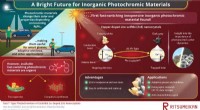
- Met koper gedoteerd zinksulfide verandert omkeerbaar van kleur wanneer het wordt verlicht en kan worden gebruikt in slimme adaptieve vensters
 Snakes of Northwest Arizona
Snakes of Northwest Arizona Wat zijn natuurlijke satellieten?
Wat zijn natuurlijke satellieten?  Kleine gereedschappen wijzen op specialistische vaardigheden van oude Indonesiërs
Kleine gereedschappen wijzen op specialistische vaardigheden van oude Indonesiërs Onderzoek toont aan dat ondergedompelde vegetatie helpt om de verzuring van Chesapeake Bay tegen te gaan
Onderzoek toont aan dat ondergedompelde vegetatie helpt om de verzuring van Chesapeake Bay tegen te gaan Hightech mysterie:is er een Facebook-telefoon in de maak?
Hightech mysterie:is er een Facebook-telefoon in de maak?  Komt breking op wanneer licht door een stuk glas gaat?
Komt breking op wanneer licht door een stuk glas gaat?  COVID-19:Economische impact, menselijke oplossingen
COVID-19:Economische impact, menselijke oplossingen Zorgen voor stabiliteit op lange termijn van pesticiden in honing
Zorgen voor stabiliteit op lange termijn van pesticiden in honing
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

