
Wetenschap
Heeft chloor een hoger kookpunt dan jodium?
Dit is waarom:
* intermoleculaire krachten: De sterkte van intermoleculaire krachten tussen moleculen bepaalt het kookpunt. Jodium heeft sterkere dispersietroepen in Londen (een type van der Waals -kracht) dan chloor vanwege de grotere omvang en een groter aantal elektronen.
* Grootte en polariseerbaarheid: Jodiumatomen zijn veel groter dan chlooratomen. Dit betekent dat ze meer polariseerbaar zijn, wat betekent dat hun elektronenwolken gemakkelijker kunnen worden vervormd. Grotere polariseerbaarheid leidt tot sterkere dispersiekrachten in Londen.
kookpunten:
* chloor (Cl2): -34.04 ° C
* jodium (i2): 184.3 ° C
Daarom vereisen de sterkere intermoleculaire krachten van jodium meer energie om te overwinnen, wat resulteert in een hoger kookpunt.
 Studie in Ethiopië koppelt gezonde bodems aan voedzamere granen
Studie in Ethiopië koppelt gezonde bodems aan voedzamere granen Een focus op eerlijkheid:onderzoek onderzoekt hoe kinderen reageren op ongelijkheid over de hele wereld
Een focus op eerlijkheid:onderzoek onderzoekt hoe kinderen reageren op ongelijkheid over de hele wereld  Wat zijn de vier ecosysteemtypen?
Wat zijn de vier ecosysteemtypen?  Nieuwe studie onthult dat Ulsan jarenlang wordt blootgesteld aan giftig fijnstof
Nieuwe studie onthult dat Ulsan jarenlang wordt blootgesteld aan giftig fijnstof Welke menselijke acties bedreigen het voortbestaan van bossen?
Welke menselijke acties bedreigen het voortbestaan van bossen?
Hoofdlijnen
- Hoe je robots ter grootte van een cel massaal kunt produceren
- Planten bevatten een stof die bekend staat als wat niet kan worden verteerd door koe?
- COVID-19-virus verstoort de eiwitproductie:onderzoeker bespreekt haar recente bevindingen
- Bronnen van het lactase-enzym
- Waarom sommige vuurvliegjes femme fatales worden in hun race om te overleven
- Hoe biologen veldwerk veiliger en rechtvaardiger maken
- Welk organisme is een herbivoor?
- Onderzoeker:De werkelijke kosten van voedsel zijn veel hoger dan wat u aan de kassa uitgeeft
- Dolfijn uit Florida gevonden met hoogpathogene vogelgriep:rapport
- Nieuw materiaal om wonden te behandelen kan beschermen tegen resistente bacteriën
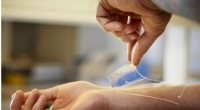
- Onderzoeksteam maakt hydrogellijmen om wonden af te dichten

- Onderzoekers gebruiken jiggly Jell-O om krachtige nieuwe waterstofbrandstofkatalysator te maken
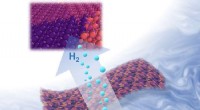
- Magnetische tanden zijn veelbelovend voor materialen en energie

- In baanbrekende methode om zonnemateriaal te creëren, NREL-wetenschappers bewijzen dat het onmogelijke echt niet is

 Röntgenexperimenten suggereren een hoge afstembaarheid van 2D-materiaal
Röntgenexperimenten suggereren een hoge afstembaarheid van 2D-materiaal 25 cm is gelijk aan hoeveel inches?
25 cm is gelijk aan hoeveel inches?  Wat is het veiligste zuur of alkali?
Wat is het veiligste zuur of alkali?  Wat is het product van de massa van een voorwerp maal zijn snelheid?
Wat is het product van de massa van een voorwerp maal zijn snelheid?  Singapore Airlines ontkent snuffelen met camera's op de rugleuning
Singapore Airlines ontkent snuffelen met camera's op de rugleuning Wat is de fase van de celcyclus bij het voorbereiden om zich te voortplanten?
Wat is de fase van de celcyclus bij het voorbereiden om zich te voortplanten?  Een natriumatoom verliest gemakkelijk een elektron in een chemische reactie Wat duidt dit op het vermogen om oplossingen te vormen?
Een natriumatoom verliest gemakkelijk een elektron in een chemische reactie Wat duidt dit op het vermogen om oplossingen te vormen?  Wat is de pH van verschillende soorten theebladeren?
Wat is de pH van verschillende soorten theebladeren?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

