
Wetenschap
Hoe veranderden de resultaten van JJ -experimenten hoe wetenschappers aan atomen dachten?
Voor de experimenten van Thomson:
* Dalton's atomaire theorie: Vóór Thomson was het heersende model van het atoom de theorie van John Dalton. Deze theorie stelde voor dat atomen ondeelbare, vaste bollen waren.
* Geen kennis van subatomaire deeltjes: Wetenschappers hadden geen concept van kleinere deeltjes in het atoom, zoals elektronen, protonen of neutronen.
Thomson's experimenten en hun impact:
* Ontdekking van het elektron: Thomson's experimenten toonden het bestaan van negatief geladen deeltjes, die hij elektronen noemde. Dit was een grote doorbraak, waaruit blijkt dat atomen niet ondeelbaar waren.
* pruimpuddingmodel: Op basis van zijn experimenten stelde Thomson het "pruimpuddingmodel" van het atoom voor. Dit model stelde het atoom voor als een bol van positief geladen materiaal, met negatief geladen elektronen ingebed als pruimen in een pudding.
* atoom is niet solide: Het werk van Thomson toonde aan dat atomen een interne structuur hadden en niet alleen solide bollen waren. Dit daagde het vorige begrip van het atoom uit.
gevolgen van het nieuwe begrip:
* atoom als een complex systeem: De ontdekking van het elektron opende de deur voor een complexer uitzicht op het atoom. Wetenschappers begonnen de mogelijkheid van andere subatomaire deeltjes te onderzoeken en hoe ze interactie hadden.
* Foundation voor toekomstige ontdekkingen: Thomson's werk maakte de weg vrij voor latere experimenten, zoals Rutherford's Gold Foil -experiment, wat leidde tot de ontwikkeling van het nucleaire model van het atoom.
Samenvattend:
J.J. Thomson's experimenten hebben ons begrip van het atoom fundamenteel veranderd. Hij bewees dat atomen niet ondeelbaar waren en interne structuur hadden. Deze ontdekking leidde tot de ontwikkeling van nieuwe atoommodellen en stimuleerde verder onderzoek naar het fundamentele karakter van materie.
 Universiteit van Minnesota meldt doorbraak in 3D-printen voor herstel van het ruggenmerg
Universiteit van Minnesota meldt doorbraak in 3D-printen voor herstel van het ruggenmerg Materialen door welke warmte kan gemakkelijk stromen worden opgeroepen?
Materialen door welke warmte kan gemakkelijk stromen worden opgeroepen?  Wanneer zout oplost in water, wat is de opgeloste stof en het oplosmiddel?
Wanneer zout oplost in water, wat is de opgeloste stof en het oplosmiddel?  Krijt scheiden van een mengsel van een kopersulfaatoplossing?
Krijt scheiden van een mengsel van een kopersulfaatoplossing?  Synthesiereacties zijn vooral belangrijk in het lichaam voor?
Synthesiereacties zijn vooral belangrijk in het lichaam voor?
 Seismologen bieden gedetailleerde kijk op de aardbeving in Kaikoura in Nieuw-Zeeland
Seismologen bieden gedetailleerde kijk op de aardbeving in Kaikoura in Nieuw-Zeeland Klimaatverandering zorgt voor bosbranden, en niet alleen in Californië
Klimaatverandering zorgt voor bosbranden, en niet alleen in Californië Wetenschappers kwantificeren de wereldwijde vulkanische CO2-ontluchting; schatting totale koolstof op aarde
Wetenschappers kwantificeren de wereldwijde vulkanische CO2-ontluchting; schatting totale koolstof op aarde Miljard jaar oude meerafzetting levert aanwijzingen voor de oude biosfeer van de aarde
Miljard jaar oude meerafzetting levert aanwijzingen voor de oude biosfeer van de aarde Onderzoek onthult het mysterieuze leven van narwallen
Onderzoek onthult het mysterieuze leven van narwallen
Hoofdlijnen
- Wat werd het raster gebruikt om overervingpatronen op basis van genotype -ouders die werden genoemd?
- Hoe een genmutatie leidt tot hogere intelligentie
- Wat zijn functies van mitose die kinderen kunnen weten?
- Wat is hypothese?
- Opsommen minimaal 12 takken van de wetenschap?
- Welke oranismen hebben de meeste kenmerken gemeen met leden van een soort of leden van een orde?
- De eerste warmbloedige dinosaurussen zijn mogelijk 180 miljoen jaar geleden ontstaan
- 10 fascinerende feiten over de nieuwe levensboom-evolutiekaart
- In welke categorieën zijn biosferen opgesplitst?
- Een nieuwe sensor voor licht, warmte en aanraking

- Beton met verbeterd slagvastheid voor verdedigingsconstructies

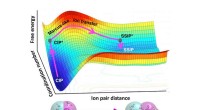
- Elegante theorie laat zien hoe water helpt bij het scheiden van ionen die betrokken zijn bij materiaalsynthese en productie
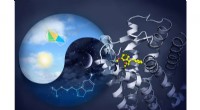
- Onderzoekers maken de eerste kaarten van twee melatoninereceptoren die essentieel zijn voor slaap
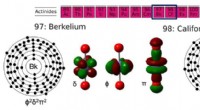
- Zeer zware elementen leveren meer elektronen
 Waarom de autoverkoop sterk is in de VS (update)
Waarom de autoverkoop sterk is in de VS (update)  In de mangoestenmaatschappij immigranten zijn een bonus - als ze tijd krijgen om zich te vestigen
In de mangoestenmaatschappij immigranten zijn een bonus - als ze tijd krijgen om zich te vestigen De kracht van gebed?
De kracht van gebed?  Waarom schijnt de maan vanavond zo fel?
Waarom schijnt de maan vanavond zo fel?  Opwarming van de aarde zorgt voor meer opwarming, nieuwe paleoklimaatstudie vindt
Opwarming van de aarde zorgt voor meer opwarming, nieuwe paleoklimaatstudie vindt VW zegt Duitse boete van 1 miljard euro te betalen voor fraude met emissies
VW zegt Duitse boete van 1 miljard euro te betalen voor fraude met emissies Hoeveel chromosomen zijn er in elke somatische cel?
Hoeveel chromosomen zijn er in elke somatische cel?  Wanneer was van kleine dingen grote groei gecreëerd?
Wanneer was van kleine dingen grote groei gecreëerd?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

