
Wetenschap
Hoeveel atomen zijn er in 68,0 kg?
* atomen hebben verschillende massa's: Elk element heeft een andere atoommassa. Een koolstofatoom is bijvoorbeeld veel lichter dan een gouden atoom.
* massa is een maat voor de hoeveelheid materie: 68,0 kg vertegenwoordigt een specifieke hoeveelheid materie, maar het vertelt ons niet wat voor soort materie.
Om het aantal atomen te berekenen, moet u:
1. De chemische formule van de stof: Dit vertelt u welke elementen aanwezig zijn en in welke verhouding.
2. Avogadro's nummer: Deze constante relateert het aantal atomen in een mol (6.022 x 10^23 atomen/mol).
Hier is hoe u het zou doen:
1. Bereken het aantal mol: Verdeel de massa (68,0 kg) door de molaire massa van de stof.
2. Vermenigvuldig met het nummer van Avogadro: Dit geeft je het aantal atomen in die vele mol.
Voorbeeld:
Stel dat u het aantal atomen in 68,0 kg puur goud (AU) wilt vinden.
1. Goudmassa (au): 196,97 g/mol
2. Converteer kg naar g: 68,0 kg * 1000 g/kg =68000 g
3. Bereken mol: 68000 g / 196,97 g / mol =345.2 mol
4. Bereken atomen: 345.2 mol * 6.022 x 10^23 atomen/mol = 2.08 x 10^26 atomen
Samenvattend moet u de specifieke stof kennen om het aantal atomen in een bepaalde massa te bepalen.
 Wetenschappers ontdekken de grootste zeewierbloei ter wereld
Wetenschappers ontdekken de grootste zeewierbloei ter wereld Na de verwoesting van de cycloon, terug naar af voor Mozambiques Beira
Na de verwoesting van de cycloon, terug naar af voor Mozambiques Beira Het land van het Vega Granada-gebied zakt tot één centimeter per jaar in als gevolg van de droogte
Het land van het Vega Granada-gebied zakt tot één centimeter per jaar in als gevolg van de droogte Klimaatverandering eist de helderheid van het water van Lake Tahoe
Klimaatverandering eist de helderheid van het water van Lake Tahoe De temperatuur in Delhi bereikt de hoogste temperatuur ooit in India:weerbureau
De temperatuur in Delhi bereikt de hoogste temperatuur ooit in India:weerbureau
Hoofdlijnen
- Waarin handelen enzymen?
- Kleine bijen spelen een grote rol in het geheime seksleven van bomen
- Waarom wordt overdracht RNA genaamd RNA?
- Hoe worden paddenstoelen magisch?
- Wat is een bio -engineer?
- Wat zijn de functies van cellenmembraan?
- Stijgende kwikniveaus kunnen bijdragen aan de afnemende populaties Steller-zeeleeuwen
- Welk proces gebruiken cellen als ze niet genoeg zuurstof hebben voor de ademhaling?
- Wat zijn cocci die zich voordoen in clusters of groepen die worden genoemd?
- Krachtveldanalyse geeft aanwijzingen voor eiwit-ion-interactie
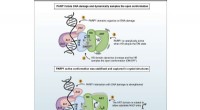
- Onderzoekers krijgen nieuwe inzichten in een dynamisch eiwit gericht op kankertherapie
- Kopercoating op 3D-geprinte plastic filters voorgesteld als een pandemische strijder

- Door nieuwe technologie kunnen belangrijke metalen efficiënter worden gemaakt

- Computermodel kan wetenschappers helpen uit elkaar te gaan, eiwitten opnieuw samenstellen op commando

 Voordelen en nadelen van digitale meters versus Analoge meters
Voordelen en nadelen van digitale meters versus Analoge meters Structuur van het spierstelsel
Structuur van het spierstelsel  Nucleaire oorlog kan een grote hap uit de zeevruchten ter wereld nemen
Nucleaire oorlog kan een grote hap uit de zeevruchten ter wereld nemen Welk gebied ervaart de kleinste seizoensgebonden variatie in zonne -energie -energie?
Welk gebied ervaart de kleinste seizoensgebonden variatie in zonne -energie -energie?  Hoeveel landen zijn er op de maan?
Hoeveel landen zijn er op de maan?  Wat is het beste milieuwetenschapsproject?
Wat is het beste milieuwetenschapsproject?  Snapchat lanceert nieuwe tools voor ontwikkelaars, het maken van AR-filters gemakkelijker maken voor beginners
Snapchat lanceert nieuwe tools voor ontwikkelaars, het maken van AR-filters gemakkelijker maken voor beginners Hoe wordt een gewas genaamd waar het erfelijkheidsmateriaal kunstmatig is veranderd om hun opbrengst te verhogen?
Hoe wordt een gewas genaamd waar het erfelijkheidsmateriaal kunstmatig is veranderd om hun opbrengst te verhogen?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

