
Wetenschap
Wat maakt een gas en het is niet vloeibaar of vast?
Belangrijkste verschillen:
* deeltjesopstelling en beweging:
* gas: Deeltjes zijn breed op elkaar geplaatst, bewegen vrij en hebben hoge kinetische energie. Ze botsen constant met elkaar en de muren van hun container.
* vloeistof: Deeltjes zijn dichter bij elkaar dan in een gas, maar hebben nog steeds enige bewegingsvrijheid. Ze vertonen vloeiend gedrag.
* solide: Deeltjes zijn strak verpakt in een vaste opstelling, trillend op zijn plaats maar niet in staat om vrij te bewegen.
* Vorm en volume:
* gas: Neemt de vorm en het volume van zijn container aan.
* vloeistof: Heeft een duidelijk volume maar neemt de vorm van zijn container aan.
* solide: Heeft een duidelijke vorm en volume.
* Compressibiliteit:
* gas: Zeer samendrukbaar, omdat de deeltjes veel ruimte hebben tussen hen.
* vloeistof: Relatief niet -samendrukbaar, omdat de deeltjes dichter bij elkaar zijn.
* solide: In wezen onvergimeld.
Samenvattend:
Het bepalende kenmerk van een gas is de zwakke intermoleculaire krachten tussen zijn deeltjes. Hierdoor kunnen ze vrij bewegen, elke ruimte die ze innemen vullen en gemakkelijk worden gecomprimeerd. Vloeistoffen hebben sterkere intermoleculaire krachten, houden deeltjes dichter bij elkaar, terwijl vaste stoffen de sterkste krachten hebben en deeltjes in een rigide structuur vergrendelen.
 Wat wordt er gemaakt van twee of meer stoffen die chemisch aan elkaar verbonden zijn?
Wat wordt er gemaakt van twee of meer stoffen die chemisch aan elkaar verbonden zijn?  Hoe kunnen de oplosbaarheidsregels helpen het product van een reactie te voorspellen?
Hoe kunnen de oplosbaarheidsregels helpen het product van een reactie te voorspellen?  Welke chemische stof is vergelijkbaar met uranium?
Welke chemische stof is vergelijkbaar met uranium?  Wetenschappers stellen een dynamische ladings- en oxidatietoestand voor voor katalysatoren met één atoom
Wetenschappers stellen een dynamische ladings- en oxidatietoestand voor voor katalysatoren met één atoom In welke toestand verkeert stikstof?
In welke toestand verkeert stikstof?
 Werelderfgoedlocaties bedreigd door zeespiegelstijging
Werelderfgoedlocaties bedreigd door zeespiegelstijging NASA-gegevens helpen ozongaten op weg naar herstel
NASA-gegevens helpen ozongaten op weg naar herstel Hoe Caterpillar schrankladers en multi-terrain werken
Hoe Caterpillar schrankladers en multi-terrain werken  LA's grootste aardbevingsdreiging bevindt zich op een over het hoofd gezien deel van San Andreas, studie zegt. Dat kan goed zijn
LA's grootste aardbevingsdreiging bevindt zich op een over het hoofd gezien deel van San Andreas, studie zegt. Dat kan goed zijn Gevangenisstraffen voor Franse oplichters in koolstofhandel
Gevangenisstraffen voor Franse oplichters in koolstofhandel
Hoofdlijnen
- Het enige bloedgroep dat kan worden gebruikt zonder het gevaar dat antilichamen zijn rode cellen klonteren is?
- Wat zijn de 4 hoofdonderdelen van een virus?
- Hoe eiwitten hun plaats in de cel vinden
- Wat wordt voornamelijk aangetroffen in mitochondria lydsosoom ridosoom of Golgi -complexen van dierencellen?
- Hoe hersendood werkt
- Dit zijn de basisbouwstenen van eiwitten?
- Hoeveel markers worden gebruikt om een DNA -profiel te maken?
- Voedden primitieve walvisachtigen zich als zeereptielen?
- Waar bevindt de kern zich in een plantencel?
- Biogefunctionaliseerd keramiek voor herstel van schedelbotdefecten - in vivo onderzoek

- Nieuwe manieren ontwikkelen om de koperproductie te bevorderen
- Video:Hoe kimchi zijn kick krijgt

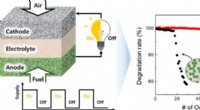
- Lager nikkelgehalte en verbeterde stabiliteit en prestaties in keramische brandstofcellen
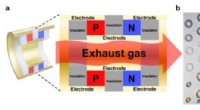
- Een thermo-elektrische inkt die uitlaatpijpen van auto's verandert in stroomgeneratoren
 Het hebben van meer bondgenoten kan de macht van een land verminderen
Het hebben van meer bondgenoten kan de macht van een land verminderen Nieuw platform zet traditionele on-demand supply chain-aanpak op zijn kop
Nieuw platform zet traditionele on-demand supply chain-aanpak op zijn kop Is de zon ooit direct boven het hoofd in de zomer van Australië?
Is de zon ooit direct boven het hoofd in de zomer van Australië?  Wat is de beweging van fragmenten rock?
Wat is de beweging van fragmenten rock?  Blauwe fosfor:hoe een halfgeleider een metaal wordt
Blauwe fosfor:hoe een halfgeleider een metaal wordt Nettowinst Sony eerste kwartaal lager door eenmalige factoren
Nettowinst Sony eerste kwartaal lager door eenmalige factoren Hoe leer je High School Math Online
Hoe leer je High School Math Online Wat is het verschil tussen met de klok mee en tegengesteld?
Wat is het verschil tussen met de klok mee en tegengesteld?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

