
Wetenschap
Biogefunctionaliseerd keramiek voor herstel van schedelbotdefecten - in vivo onderzoek
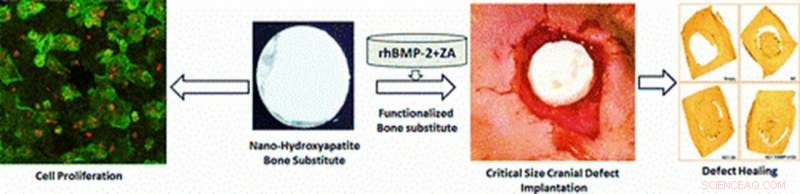
Illustratie van de multifunctionele materialen die experimenteel zijn ontwikkeld in de studie voor in vivo toepassingen van celproliferatie en cranioplastiek. Genezing van defecten in een knaagdiermodel wordt waargenomen na 12 weken scaffold-implantatie op de plaats van defect met celproliferatie, radiografie, micro-CT en histologische analyses. Afbeelding tegoed:ACS Applied Materials &Interfaces. Credit: Multifunctionele materialen , doi:https://doi.org/10.1088/2399-7532/aafc5b
Vooruitgang in materiaalwetenschap en productietechnologie hebben strategieën voor botweefselengineering (BTE) mogelijk gemaakt die complexe steigers met gecontroleerde architectuur voor botherstel genereren. De nieuwe biomaterialen kunnen verder worden gefunctionaliseerd met bioactieve moleculen voor biocompatibiliteit door osteo-inductiviteit te verbeteren (osteogenese induceren om botgenezing te initiëren). In een recente studie gepubliceerd in multifunctionele materialen, IOP Wetenschap , Arun Kumar Teotia en medewerkers van de afdelingen bio-engineering, orthopedie, chemische technologie en biomedische technologie, in India, Finland en Zweden ontwikkelden een roman, multifunctioneel, dubbellaagse composietsteiger (BCS). Het nieuwe materiaal bevatte keramisch nanocement (NC) en de macroporeuze composietsteiger (CG) om de botarchitectuur na te bootsen tijdens botherstel.
Om de steigers te functionaliseren, de materiaalwetenschappers voegden recombinant humaan bot morfogenetisch eiwit-2 (rhBMP-2) (BMP) en zoledroninezuur (ZA) toe. De wetenschappers stelden voor dat de samengestelde steigers de proliferatie van osteoblast-voorlopercellen zouden ondersteunen, naast de gecontroleerde afgifte van geladen bioactieve moleculen om botregeneratie te induceren. Wetenschappers in hetzelfde onderzoeksteam hadden eerder een soortgelijk multifunctioneel materiaal ontwikkeld om de initiële impact ervan te testen tijdens een in vivo pilootstudie.
In de huidige studie, Teotia et al. waargenomen een grotere hoeveelheid gemineraliseerd weefsel (MT) met gefunctionaliseerde steigers binnen 12 weken na in vivo implantatie in een grotere groep ratten met 8,5 mm kritische schedeldefecten. De gecombineerde dubbellaagse composietsteigers (BCS) gefunctionaliseerd met zoledroninezuur (ZA) (om BCS + ZA te vormen) bevatten de hoogste MT-afzetting (13,9 mm 3 ). Gevolgd door de macroporeuze composietsteiger (CG) gefunctionaliseerd met BMP en ZA (CG+BMP+ZA) op 9,2 mm 3 en BCS+ZA+BMP met 7,6 mm 3 van MT deponering.
De MT-waarden die in het onderzoek tijdens botregeneratie werden geregistreerd, waren significant hoger dan de osteogenesepercentages op de niet-gefunctionaliseerde CG- of BCS-steigers alleen (zonder bioactieve moleculen). De resultaten ondersteunen de AHO-strategieën die in het onderzoek zijn ontwikkeld om een osteo-bevorderende multifunctionele steiger te vormen die in vivo kan worden geïmplanteerd om kritieke defecten te herstellen.
Een uniek kenmerk van botweefsel is het vermogen om te genezen zonder littekenvorming als een zeer dynamisch weefsel met een aanzienlijk potentieel voor regeneratie. Natuurlijke botvorming vindt plaats via endochondrale ossificatie in buisvormige botten (bijv. vingerkootjes, femur) of tijdens kraakbeenafzetting, gevolgd door ossificatie. In een derde proces intramembraneuze directe ossificatie kan optreden in platte botten (schedel, bekken) zonder kraakbeenvorming. Regeneratie is een langzaam proces in platte botten (schedel, bekken) als gevolg van beperkte mesenchymale stamcellen (MSC's), waarvoor grote celrekrutering uit het periosteum of de dura nodig is.
Als resultaat, genezing van kritieke groottedefecten in platte botten, zoals de schedel is een uitdaging die geoptimaliseerde AHO-strategieën vereist. Autograft botflappen hadden aanvankelijk de voorkeur voor cranioplastiek om immunologische reacties te minimaliseren, infecties en herkenning van vreemde lichamen. Daarna, wetenschappers ontwikkelden gevasculariseerde calvariumbottransplantaten als een voorkeurskeuze voor schedelreconstructie in aanvullende studies. Echter, de bijbehorende transplantatiestrategieën zorgden voor complicaties tijdens materiaalresorptie na implantatie en reparatie, naast andere klinische complicaties op de contactplaats tussen het implantaat en het oorspronkelijke bot. Regeneratie en celinfiltratie in een calvaria-flap hangt grotendeels af van voorlopercellen die kunnen migreren van de onderliggende dura of de bovenliggende pericraniale lagen, differentiëren tot actieve osteogene cellen voor genezing. Als celmigratie wordt afgesloten van de twee membranen (dura en pericranium), botvorming aanzienlijk lager zou zijn.
Wetenschappers hadden al vastgesteld dat de twee membranen belangrijk zijn bij het spelen van een specifieke rol tijdens regeneratie, hoewel met de leeftijd de rol van het periosteum bij de regeneratie van de schedel minder belangrijk is. In de huidige studie, Teotia et al. ontwikkelde de hypothese dat een osteoconductief oppervlak overspraak tussen de dura en pericraniale lagen zou kunnen behouden voor vroege vascularisatie en klinisch succes. Om dit te bereiken, ze genereerden een tweelagige steigerarchitectuur die een resorbeerbaar bifasisch nano-hydroxyapatiet-calciumsulfaat keramisch nanocement (NC) in de bovenste laag en zijde-bioglas-hydroxyapatiet composiet poreuze cryogel (CG) als een onderliggende laag integreerde.
Teotia et al. het dubbelgelaagde ontwerp gebruikt om de mechanische sterkte van NC te integreren als een beschermende bovenlaag en de poreuze composiet CG-laag als een oppervlak voor celbevestiging, infiltratie, proliferatie en vascularisatie. De wetenschappers verwachtten dat de ontworpen oppervlakken de communicatie tussen de onderliggende dura en de bovenliggende periostale membranen zouden behouden. Ze functionaliseerden de nieuwe materialen en implanteerden ze in vivo in Wistar-ratten met kritieke schedeldefecten om het effect van tweelagige poreuze architectuur op osteoconductie en botvorming in preklinische, translationele studies.
Tijdens de fabricage van materialen, de wetenschappers wierpen de NC in een concaaf-convexe architectuur om te passen bij de vorm van de schedel en lieten het uitharden, om multifunctionele dubbellaagse steigers te ontwerpen voor cranioplastiek. Ze vormden cirkelvormige BCS-schijven bestaande uit bovenste NC en onderste CG en voerden chirurgische procedures uit op de diermodellen. Tijdens de operatie, Teotia et al. implanteerde de scaffold-schijven op de plaats van het defect en voerde ex vivo micro-CT en radiologische analyse uit op het uitgesneden en geoogste calvarium na het opofferen van de diermodellen, 12 weken na schijfimplantatie.
De wetenschappers voltooiden radiologische analyses van botvorming op de plaats van het defect om de vorming van verbeend weefsel waar te nemen, met behulp van de nanoScan in vivo scanner voor radiografische projecties van het defect. Ze gebruikten micro-CT-analyse om de vorming van sterk gemineraliseerd weefsel (MT) te detecteren en het vullen van defecten in het chirurgisch geïnduceerde cirkeldefect van 8,5 mm (interessegebied) te onderzoeken. Tegen 12 weken, mineralisatie bereikte geen perfecte sluiting in het diermodel. De wetenschappers gebruikten beeldkwantificerende software om de hoogste hoeveelheid gemineraliseerde weefselvorming in de BCS+ZA-groep aan te tonen, gevolgd door de groep CG+ZA+BMP, gevolgd door CG+ZA+BMP en BCS+ZA+BMP groepen.
Na de oogst, de wetenschappers repareerden de schedelmonsters voor histologische analyse en voerden hematoxyline en eosine (H&E) en Masson's trichroomkleuring van rattencalvarias uit. Ze toonden aan dat zowel de poreuze composiet scaffold (CG) als de bilayered scaffold (NC+GC) (BCS) goed integreerden met bestaand bot op de plaats van het defect. De steigers zorgden voor poreuze oppervlakken voor grondige celinfiltratie. Teotia et al. toonde ook aan dat gefunctionaliseerde scaffolds consistent hogere MT-vorming hadden via histologie-assays vanwege de aanwezigheid van osteoconductieve en osteo-inductieve factoren in de bioactieve moleculensamenstelling in vergelijking met de niet-gefunctionaliseerde groepen. De histologische resultaten waren consistent met de micro-CT-resultaten in het onderzoek.
Op deze manier, Teotia et al. toonde aan dat multifunctionele composietsteigers auto- of allografts in grote afmetingen kunnen vervangen, botdefecten in de schedel. Ze toonden aan dat de multifunctionele materialen in staat waren om vroege vascularisatie te induceren en mineralisatie in vivo te verbeteren. Zoals verwacht, de composietsteigers maakten poreuze osteoconductieve communicatie mogelijk tussen vroege celinfiltratie vanuit het periosteum en de onderliggende dura-lagen tijdens snelle botvorming. De multifunctionele materialen zijn veelbelovend voor het verbeteren van botmineralisatie en vroege genezing van defecten na implantatie. Teotia et al. voorstellen om aanvullende studies uit te voeren in grote preklinische diermodellen om het nieuwe biomateriaal te optimaliseren en te vertalen voor klinische toepassingen.
© 2019 Wetenschap X Netwerk
 Doorstroomelektroden maken waterstof 50 keer sneller
Doorstroomelektroden maken waterstof 50 keer sneller Wetenschappers ontwikkelen nieuwe verbinding die beide soorten antibioticaresistente superbacteriën doodt
Wetenschappers ontwikkelen nieuwe verbinding die beide soorten antibioticaresistente superbacteriën doodt Hoe maak je nep sneeuw met bakken Soda
Hoe maak je nep sneeuw met bakken Soda Sporen van meerdere klassen antibiotica in voedingsmiddelen detecteren
Sporen van meerdere klassen antibiotica in voedingsmiddelen detecteren Lijst van de componenten van een Photosystem
Lijst van de componenten van een Photosystem
 De Dode Zee – milieuonderzoek op de rand van uitersten
De Dode Zee – milieuonderzoek op de rand van uitersten Vrees op zeeniveau omdat er meer gigantische Antarctische gletsjer drijft dan gedacht
Vrees op zeeniveau omdat er meer gigantische Antarctische gletsjer drijft dan gedacht Het belang van het broeikaseffect
Het belang van het broeikaseffect  NASA krijgt infraroodbeeld van Carolina Chris, de tropische storm
NASA krijgt infraroodbeeld van Carolina Chris, de tropische storm Is toenemend kunstlicht 's nachts een gevaar voor koraalriffen?
Is toenemend kunstlicht 's nachts een gevaar voor koraalriffen?
Hoofdlijnen
- Hoe is een Paramecium Digest Food?
- Samenstelling van de celwand van de zes koninkrijken
- Hoge prijzen van dierlijke producten onderdeel van een vicieuze cirkel naar uitsterven
- Nieuw onderzoek dat kankerremmende eiwitten koppelt aan celantennes
- De rol van ribosomen in Homeostasis
- Invasieve wormen verspreiden zich in arboretumbossen, beperkte effecten tot nu toe
- Wormsoorten verloren 7, 000 genen na evolutie om zichzelf te bevruchten
- De effecten van straling op dieren
- Waarom doden we?
- Robotchemicus ontdekt nieuwe moleculen en reacties

- Van twee kanten naar moleculen kijken met femtoseconde zachte röntgenstralen op tafel

- Wetenschappers observeren hoe potentiële kankerbehandeling reageert in een enkele cel
- Biomarkers die kunnen helpen bepalen wie risico loopt op ernstige COVID-19-symptomen

- Onderzoekers ontwerpen een superkatalysator om kunststoffen en brandstoffen te produceren zonder ruwe olie
 Hoe planten planten met sporen zich voort?
Hoe planten planten met sporen zich voort?  Trilobiet opgroeien
Trilobiet opgroeien Specificaties Ford Backhoe
Specificaties Ford Backhoe  NASA vangt de geboorte van de tropische storm Francisco in de Noordwestelijke Stille Oceaan
NASA vangt de geboorte van de tropische storm Francisco in de Noordwestelijke Stille Oceaan T-Mobile laat je de service een maand lang uitproberen met je eigen telefoon en nummer - gratis
T-Mobile laat je de service een maand lang uitproberen met je eigen telefoon en nummer - gratis Vermist in lockdown - nieuw rapport onthult dat de kwetsbaren meer risico lopen
Vermist in lockdown - nieuw rapport onthult dat de kwetsbaren meer risico lopen Kettinglengte bepaalt moleculaire kleur, kleurafstemming voor medische beeldvorming mogelijk maken
Kettinglengte bepaalt moleculaire kleur, kleurafstemming voor medische beeldvorming mogelijk maken Antarctica zal waarschijnlijk een snelle zeespiegelstijging veroorzaken onder klimaatverandering
Antarctica zal waarschijnlijk een snelle zeespiegelstijging veroorzaken onder klimaatverandering
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

