
Wetenschap
Hoe vertegenwoordigen wetenschappers chemische elementen?
1. Chemische symbolen:
- meest voorkomende en fundamentele methode.
- Elk element krijgt een uniek een of twee lettersymbool, meestal afgeleid van de Latijnse of Engelse naam.
- Voorbeeld:waterstof (h), zuurstof (o), koolstof (c), goud (au), uranium (u).
2. Atomisch nummer:
- vertegenwoordigt het aantal protonen in de kern van een atoom.
- Definieert het element en zijn positie op het periodiek systeem.
- Vertegenwoordigd door een heel getal.
- Voorbeeld:waterstof (atoomnummer 1), zuurstof (atoomnummer 8), koolstof (atoomnummer 6).
3. Atomic Mass:
- Gemiddelde massa van een atoom van dat element, rekening houdend met de isotopen.
- uitgedrukt in atomaire massa -eenheden (AMU).
- Voorbeeld:waterstof (1.008 AMU), zuurstof (15.999 AMU), koolstof (12.011 AMU).
4. Periodic tabel:
- Organiseert elementen op basis van hun atoomnummer en terugkerende eigenschappen.
- toont de relaties tussen elementen, waardoor hun reactiviteit en gedrag worden voorspeld.
5. Elektronenconfiguratie:
- beschrijft de opstelling van elektronen in de energieniveaus van een atoom.
- Gebruikt om chemische binding en reactiviteit te begrijpen.
- Voorbeeld:waterstof (1S1), zuurstof (1S2 2S2 2P4), koolstof (1S2 2S2 2p2).
6. Nucleaire symbolen:
- vertegenwoordigt de specifieke isotoop van een element.
- Bevat het symbool van het element, het atoomnummer en het massanummer (aantal protonen plus neutronen).
-Voorbeeld:carbon-12 (¹²C), koolstof-14 (¹⁴C).
7. Elementaire formules:
- gebruikt om de samenstelling van moleculen en verbindingen weer te geven.
- toont het aantal atomen van elk aanwezige element.
- Voorbeeld:water (h₂o), koolstofdioxide (co₂), glucose (c₆h₁₂o₆).
De methode die wordt gebruikt om een element weer te geven, hangt af van de specifieke context en welke informatie moet worden overgebracht.
 Welk mineraal zou geen metalen glans hebben?
Welk mineraal zou geen metalen glans hebben?  Wat is de temperatuur bij welke kristallen zich zullen vormen wanneer een oplossing van 30 g kaliumnitraat in 100 gekoeld water?
Wat is de temperatuur bij welke kristallen zich zullen vormen wanneer een oplossing van 30 g kaliumnitraat in 100 gekoeld water?  Wat zou de kans op een reactie vergroten als twee moleculen botsen?
Wat zou de kans op een reactie vergroten als twee moleculen botsen?  Kun je minstens 5 voorbeeld geven van een gasoplossing?
Kun je minstens 5 voorbeeld geven van een gasoplossing?  Neutronen vangen vormveranderend coronavirus-eiwitcomplex op heterdaad
Neutronen vangen vormveranderend coronavirus-eiwitcomplex op heterdaad
 Waar komt het water dat we gebruiken om aan onze dagelijkse behoeften te voldoen?
Waar komt het water dat we gebruiken om aan onze dagelijkse behoeften te voldoen?  Kunstmatige intelligentie begeleidt snelle gegevensgestuurde verkenning van onderwaterhabitats
Kunstmatige intelligentie begeleidt snelle gegevensgestuurde verkenning van onderwaterhabitats Wat zijn 2 van de beste karaktereigenschappen om Charles Darwin te beschrijven?
Wat zijn 2 van de beste karaktereigenschappen om Charles Darwin te beschrijven?  Hoeveel verschil kan één graad opwarming maken?
Hoeveel verschil kan één graad opwarming maken?  Covid-19-beperkende inspanningen kunnen de VS op het goede spoor zetten om de doelstellingen van het klimaatakkoord van Parijs te halen
Covid-19-beperkende inspanningen kunnen de VS op het goede spoor zetten om de doelstellingen van het klimaatakkoord van Parijs te halen
Hoofdlijnen
- Hoe zou een nucleaire winter de voedselproductie beïnvloeden?
- Wetenschappers laten zien hoe de signaalmoleculen BMP en FGF de celdifferentiatie tijdens de embryonale ontwikkeling begeleiden
- Zijn nucleïnezuren blauwdrukken voor eiwitten?
- Wetenschappers die anatomie bestuderen?
- Experimenten laten zien dat efficiënte strategieën zich beter ontwikkelen over de generaties heen als mensen de keuze hebben over een leraar
- Wat is een netwerk van dun weefsel dat door het cytoplasma loopt en het helpt materialen naar alle celonderdelen te verplaatsen?
- Welke planten die voedsel in hun wortels opslaan, groeien mensen?
- Wat is de betekenis van het afleiden van het wetenschapsproces?
- Welk orgaan produceert enzymen die vetten en koolhydraten afbreken?
- Studie onthult continu pad naar bouwstenen van het leven

- Wetenschappers maken galactische bouwstenen om de ruimte tussen sterren te bestuderen

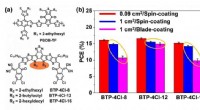
- Organische fotovoltaïsche cel met 17% efficiëntie en superieure verwerkbaarheid voor coatings op grote oppervlakken
- Zelfassemblage van zeer poreuze kristallijne deeltjes tot nieuwe fotonische materialen voor detectietoepassingen

- Nieuwe 3D-printmethode kan materiaal achter vitale medische isotoop transformeren

 Wat is de snelheid als International Space Station in een baan per uur in een baan om de aarde?
Wat is de snelheid als International Space Station in een baan per uur in een baan om de aarde?  Nieuwe online tool toont klimaatverandering in je achtertuin
Nieuwe online tool toont klimaatverandering in je achtertuin Law of Conservation Mass staat bekend als wetsuitwisselbaarheid, waarom?
Law of Conservation Mass staat bekend als wetsuitwisselbaarheid, waarom?  Ruimtewetenschappers lossen een decennialange gammaflits-puzzel op
Ruimtewetenschappers lossen een decennialange gammaflits-puzzel op Schedels laten zien dat vrouwen door middeleeuws Europa trokken, niet alleen mannen
Schedels laten zien dat vrouwen door middeleeuws Europa trokken, niet alleen mannen  Schaarste vermindert de zorgen van consumenten over prijzen, zelfs tijdens een pandemie, uit onderzoek blijkt
Schaarste vermindert de zorgen van consumenten over prijzen, zelfs tijdens een pandemie, uit onderzoek blijkt Koolstofkredieten zijn nuttig voor het stabiliseren van het klimaat, maar worden ze ook effectief gebruikt?
Koolstofkredieten zijn nuttig voor het stabiliseren van het klimaat, maar worden ze ook effectief gebruikt?  Welke subatomaire deeltjes hebben zeer weinig massa en een negatieve lading-?
Welke subatomaire deeltjes hebben zeer weinig massa en een negatieve lading-?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

