
Wetenschap
Geeft het toevoegen van coëfficiënten aan een chemische vergelijking de wet van het definiëren van verhoudingen ongehoorzaam?
Dit is waarom:
* De wet van duidelijke verhoudingen: Deze wet stelt dat een chemische verbinding altijd dezelfde elementen in dezelfde verhoudingen bevat door massa, ongeacht de bron ervan. Water (H₂o) zal bijvoorbeeld altijd twee waterstofatomen hebben voor elk zuurstofatoom.
* Balancing chemische vergelijkingen: Coëfficiënten zijn getallen geplaatst voor chemische formules in een vergelijking om ervoor te zorgen dat het aantal atomen van elk element aan de reactantzijde (links) gelijk is aan het aantal atomen van dat element aan de productzijde (rechts). Dit zorgt ervoor dat de totale massa van de reactanten gelijk is aan de totale massa van de producten, na de wet van het behoud van massa.
Voorbeeld:
Laten we eens kijken naar de verbranding van methaan:
Onevenwichtige vergelijking: Ch₄ + o₂ → co₂ + h₂o
Deze vergelijking is onevenwichtig omdat:
* Er is 1 koolstofatoom aan de reactantzijde maar 1 aan de productzijde.
* Er zijn 4 waterstofatomen aan de reactantzijde maar 2 aan de productzijde.
* Er zijn 2 zuurstofatomen aan de reactantzijde maar 3 aan de productzijde.
Balanced vergelijking: Ch₄ + 2o₂ → co₂ + 2h₂o
Door coëfficiënten toe te voegen, balanceren we de vergelijking:
* Er is 1 koolstofatoom aan elke kant.
* Er zijn 4 waterstofatomen aan elke kant.
* Er zijn 4 zuurstofatomen aan elke kant.
Conclusie: Het toevoegen van coëfficiënten in een chemische vergelijking is essentieel voor het in evenwicht brengen van de vergelijking, wat op zijn beurt ervoor zorgt dat de chemische reactie zich hecht aan de wet van bepaalde verhoudingen. De coëfficiënten vertegenwoordigen het aantal mol van elke reactant en product die bij de reactie betrokken is, zodat de massa van de reactanten en producten consistent blijft.
 Duurzaam transport:de lucht zuiveren met stikstofdoping
Duurzaam transport:de lucht zuiveren met stikstofdoping COVID-19:een wake-up call om de toeleveringsketen van geneesmiddelen opnieuw in evenwicht te brengen?
COVID-19:een wake-up call om de toeleveringsketen van geneesmiddelen opnieuw in evenwicht te brengen? Kunnen twee coniine -moleculen door London Forces interageren waarom?
Kunnen twee coniine -moleculen door London Forces interageren waarom?  Welke heeft een grotere aantrekkingskracht voor elektronenfluor of zuurstof?
Welke heeft een grotere aantrekkingskracht voor elektronenfluor of zuurstof?  Nieuwe 3D-röntgentechniek onthult geheimen van binnenuit botten
Nieuwe 3D-röntgentechniek onthult geheimen van binnenuit botten
Hoofdlijnen
- Onderscheid maken tussen organische moleculen zoals piepschuim en plastic die levende materie kenmerken?
- Langer durende ozongaten boven Antarctica stellen zeehondenpups en pinguïnkuikens bloot aan veel meer UV
- Neteldieren controleren bacteriën op afstand
- Welke klasse van biologisch molecuul bevat peptidebindingen tussen de afzonderlijke monomeren?
- Werken alle cellen precies hetzelfde?
- Nieuwe cijfers laten een bevolkingsgroei zien in de buurt van de kwetsbare koraalriffen ter wereld
- Wat is hypogeale kieming?
- Type evolutie waarin niet -gerelateerde organismen onafhankelijk overeenkomsten evolueren bij het aanpassen aan vergelijkbare omgevingen?
- Wat vormen diatomeeën zich meestal?
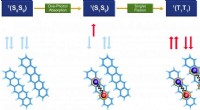
- Baanbrekende kwantumchemietechniek voor computationeel ontwerp en optimalisatie van organische fotofunctionele materialen
- Nieuw proces maakt koolstof schoner, high-performance diesel biobrandstof blendstock

- De nieuwe analysemethode in een record high-speed DNA-assayapparaat

- Hoe een COVID-19-infectie de bloedcellen op de lange termijn verandert

- Nieuwe tool ontwikkeld om auto-immuunziekten te diagnosticeren en te monitoren
 Wat betekent groei van mevrouw Gren in de wetenschapsbeschrijving?
Wat betekent groei van mevrouw Gren in de wetenschapsbeschrijving?  Onvredevolle co-existentie:hoe sterke en zwakke punten de biodiversiteit in een mierengemeenschap in stand houden
Onvredevolle co-existentie:hoe sterke en zwakke punten de biodiversiteit in een mierengemeenschap in stand houden  Welke chemische formules zouden in de natuur niet worden gevonden?
Welke chemische formules zouden in de natuur niet worden gevonden?  Uit onderzoek blijkt dat er meerdere voedingsstoffen nodig zijn om fytoplankton te laten gedijen
Uit onderzoek blijkt dat er meerdere voedingsstoffen nodig zijn om fytoplankton te laten gedijen Dieren van het ecosysteem
Dieren van het ecosysteem  Wat slimme hazmat-pakken en Sonora-cactushuiden gemeen hebben
Wat slimme hazmat-pakken en Sonora-cactushuiden gemeen hebben Feiten over Colorado State voor Kids
Feiten over Colorado State voor Kids Goed nieuws? Groenland smelt, maar minder snel dan voorspeld
Goed nieuws? Groenland smelt, maar minder snel dan voorspeld
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

