
Wetenschap
Hoeveel gram zuurstof is vereist om volledig te reageren met aluminium van 0,3 mol?
1. Schrijf de gebalanceerde chemische vergelijking:
De reactie tussen aluminium (AL) en zuurstof (O₂) produceert aluminiumoxide (Al₂o₃):
4 AL + 3 O₂ → 2 Al₂o₃
2. Bepaal de molverhouding:
De gebalanceerde vergelijking laat zien dat 4 mol aluminium reageert met 3 mol zuurstof.
3. Bereken de benodigde mol zuurstof:
* Omdat we 0,3 mol aluminium hebben, kunnen we de molverhouding gebruiken om de mol zuurstof te vinden:
(0,3 mol AL) * (3 mol O₂ / 4 mol Al) =0,225 mol O₂
4. Converteer mol zuurstof in gram:
* De molaire zuurstofmassa (o₂) is 32 g/mol.
* Vermenigvuldig de mol zuurstof met zijn molaire massa:
(0,225 mol o₂) * (32 g/mol) = 7,2 gram zuurstof
Daarom is 7,2 gram zuurstof vereist om volledig te reageren met 0,3 mol aluminium.
 Waarom kan natuurlijke selectie niet de middelen zijn waarmee een soort ontstaat?
Waarom kan natuurlijke selectie niet de middelen zijn waarmee een soort ontstaat?  Wat toont natuurlijke kenmerken van de aarde?
Wat toont natuurlijke kenmerken van de aarde?  Net zero:klimaatbesparende doelstelling of vertragingstactiek?
Net zero:klimaatbesparende doelstelling of vertragingstactiek? Waarom klimaatverandering het moeilijker maakt om mariene vervuiling te monitoren
Waarom klimaatverandering het moeilijker maakt om mariene vervuiling te monitoren Opkomende markten lopen achter in de race om groen kapitaal
Opkomende markten lopen achter in de race om groen kapitaal
Hoofdlijnen
- Waarom is de interpretatie van het resultaat belangrijk in de wetenschap?
- Welke wetenschapper ontdekte dat hitte ziektekiemen doodt?
- Waar zijn erytrocyten volwassen?
- Welke stoffen heeft het lichaam nodig om cellulaire ademhaling uit te voeren?
- Wat betekent de term alt in de wetenschap?
- Wanneer zijn genetische variaties ontstaan die ons menselijk maken?
- Onderzoekers tonen bewijs van 'geheugen' in cellen en moleculen
- Wat is het belangrijkste uitscheidingsproduct in uw lichaam?
- Waarom is ui geschikt voor DNA -extractie?
- Video:hoe Xanax werkt

- Nieuwe reactie maakt indoline-steigers beschikbaar voor farmaceutische ontwikkeling

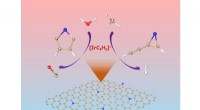
- Hoe twee isomeren van [IrC₄H₂]⁺ onafhankelijk reageren met methaan of water
- Papavers analyseren om betere medicijnen te maken

- Een bioplastic op basis van soja-eiwit dat tot 40 keer zijn eigen gewicht kan opnemen

 Hoe werden de Haïti -aardbevingsplaten genoemd?
Hoe werden de Haïti -aardbevingsplaten genoemd?  Wanneer moeten we de economie heropenen?
Wanneer moeten we de economie heropenen? Welke problemen hadden wetenschappers vóór de uitvinding van de microscoop?
Welke problemen hadden wetenschappers vóór de uitvinding van de microscoop?  Kun je het experiment tussen kwik en atmosferische druk kort uitleggen?
Kun je het experiment tussen kwik en atmosferische druk kort uitleggen?  Centrum van het Coma-cluster verkend met AstroSat
Centrum van het Coma-cluster verkend met AstroSat Californische waterbeheerders verschillen in gebruik van klimaatwetenschap
Californische waterbeheerders verschillen in gebruik van klimaatwetenschap Instagram en Threads beperken de politieke inhoud:waarom dit verschrikkelijk is voor de democratie
Instagram en Threads beperken de politieke inhoud:waarom dit verschrikkelijk is voor de democratie  Moleculaire interacties bepalen hoe nanodeeltjes zich in cellen gedragen
Moleculaire interacties bepalen hoe nanodeeltjes zich in cellen gedragen
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

