
Wetenschap
Wat zijn de edelgassen die na 1 en CL-1 lijken op hun elektronenconfiguratie?
1. Begrijp elektronenconfiguraties:
* NA (natrium): [NE] 3S¹ (Natrium heeft één valentie -elektron in de 3s orbital)
* CL (chloor): [NE] 3S² 3P⁵ (chloor heeft zeven valentie -elektronen)
2. Ionvorming:
* Na⁺ (natriumion): Verliest zijn ene valentie -elektron, wat resulteert in [NE] elektronenconfiguratie.
* CL⁻ (chloride -ion): Krijgt één elektron, wat resulteert in [AR] elektronenconfiguratie.
3. Nobelgasgelijke gelijkenis:
* Na⁺ heeft dezelfde elektronenconfiguratie als neon (ne) .
* Cl⁻ heeft dezelfde elektronenconfiguratie als argon (AR) .
Conclusie:
* Na⁺ lijkt op neon in zijn elektronenconfiguratie.
* CL⁻ lijkt op argon in zijn elektronenconfiguratie.
Dit is de reden waarom deze ionen als stabiel en niet -reactief worden beschouwd, zoals de edelgassen.
 Mandarijn van Membran is chimestry -formule?
Mandarijn van Membran is chimestry -formule?  Wat is de pH van calciumhydroxide?
Wat is de pH van calciumhydroxide?  Hoe bewaar je een ei in azijn voor een wetenschapsproject om een ei in een fles te krijgen
Hoe bewaar je een ei in azijn voor een wetenschapsproject om een ei in een fles te krijgen Wat is chloriden opladen?
Wat is chloriden opladen?  Onderzoekers infuseren bacteriën met zilver om de energie-efficiëntie in brandstofcellen te verbeteren
Onderzoekers infuseren bacteriën met zilver om de energie-efficiëntie in brandstofcellen te verbeteren
 Belang van de oostelijke woestijn in het oude Egypte
Belang van de oostelijke woestijn in het oude Egypte Kunnen nieuwe technologieën Europa helpen om insecten te proeven?
Kunnen nieuwe technologieën Europa helpen om insecten te proeven? Onderzoek naar corridors voor wilde dieren laat zien hoe deze in de loop van de tijd werken
Onderzoek naar corridors voor wilde dieren laat zien hoe deze in de loop van de tijd werken  Verre processen beïnvloeden mariene hittegolven over de hele wereld
Verre processen beïnvloeden mariene hittegolven over de hele wereld Het groeperen van slimme steden in typen kan aspirant-stadsplanners helpen een pad te vinden
Het groeperen van slimme steden in typen kan aspirant-stadsplanners helpen een pad te vinden
Hoofdlijnen
- Wat zijn alle organellen?
- Wat vormt een nucleotide?
- Wat is de overzicht van gerelateerde studies Red Cabbage?
- Wie was de 2 wetenschapper die structuur van dubbele helix -DNA ontwikkelde?
- Welke hormoon geeft verzadiging in het menselijk lichaam aan?
- Nieuwe vogelsoort genoemd naar Harvard-vader van biodiversiteit
- Achter de puppy-hondenogen
- Wat is de modellering van fylogenie A -soort?
- Nieuwe gen-editor gebruikt om ziekte in embryo's op te lossen:studie
- De verrassende kracht van vloeibare kristallen
- Nieuwe tool is bedoeld om COVID-19 te bestrijden, andere ziekten
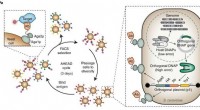
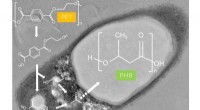
- Hoe een bacterie de plasticvervuilingscrisis kan helpen oplossen
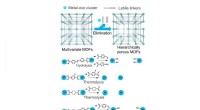
- Strategieën om grotere poriën te genereren in metaal-organische raamwerken
- Wat doet een chemische stof? Misvattingen over scheikunde aanpakken

 Google/Alphabet ziet nieuwe groei te midden van antitrustproblemen
Google/Alphabet ziet nieuwe groei te midden van antitrustproblemen Een amine en een carbonzuur reageren om water te vormen en?
Een amine en een carbonzuur reageren om water te vormen en?  Welke laag van de aarde vormt deze platen?
Welke laag van de aarde vormt deze platen?  Wat is jaloezie? Hoe verschilt jaloezie van afgunst?
Wat is jaloezie? Hoe verschilt jaloezie van afgunst?  Wetenschappers schetsen de fundamenten van een kolonie op Mars
Wetenschappers schetsen de fundamenten van een kolonie op Mars Wanneer de zonnewind de magnetosfeer van de aarde raakt, er ontstaat een verrassende stilte
Wanneer de zonnewind de magnetosfeer van de aarde raakt, er ontstaat een verrassende stilte Hoe te berekenen Hoekgrootte
Hoe te berekenen Hoekgrootte Hoe een buigpunt te vinden
Hoe een buigpunt te vinden
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

