
Wetenschap
Wat gebeurt er met het smeltpunt van alkali -metalen naarmate de atoom in grootte toeneemt?
* Metallic binding: Alkali -metalen worden bij elkaar gehouden door metalen binding, waarbij de delocalisatie van elektronen betrokken is.
* Elektronendichtheid: Naarmate de atoomgrootte toeneemt, zijn de valentie -elektronen verder weg van de kern. Dit betekent dat de elektronendichtheid in de metalen binding afneemt.
* Zwakkere aantrekkingskracht: Een lagere elektronendichtheid leidt tot zwakkere elektrostatische attracties tussen de positief geladen metaalionen en de gedelokaliseerde elektronen.
* Lager smeltpunt: Zwakkere attracties betekenen dat er minder energie nodig is om de bindingen te verbreken en het metaal te smelten. Daarom hebben grotere alkali -metalen lagere smeltpunten.
Voorbeeld:
* Lithium (Li) heeft de kleinste atomaire straal en het hoogste smeltpunt (180,5 ° C).
* Cesium (CS) heeft de grootste atoomradius en het laagste smeltpunt (28,4 ° C).
Deze trend is consistent in de gehele alkali -metaalgroep.
 Hevige winterstorm in VS neemt af
Hevige winterstorm in VS neemt af NASA ziet tropische cycloon Debbie vormen en versterken
NASA ziet tropische cycloon Debbie vormen en versterken Waarom gieren belangrijk zijn, en wat we verliezen als ze weg zijn
Waarom gieren belangrijk zijn, en wat we verliezen als ze weg zijn  De twee (land)kanten van bossen:hoe beïnvloedt het overheidsbeleid het natuurbehoud?
De twee (land)kanten van bossen:hoe beïnvloedt het overheidsbeleid het natuurbehoud?  Victoria verbiedt fracking voorgoed maar heft stilletjes het verbod op gasexploratie op land op
Victoria verbiedt fracking voorgoed maar heft stilletjes het verbod op gasexploratie op land op
Hoofdlijnen
- Wat bepaalt welke eiwitten de cel maakt?
- Van vis tot mens:onderzoek laat zien hoe vinnen benen werden
- Wat is de klasse voor dieren?
- Hoe verlaat een groot deeltje de cel door actief transport?
- Wat voor soort aseksuele reproductie wordt voortplanting zonder dat hun eieren worden bevrucht?
- Hoe reguleren PA-, ABA- en CBF-routes synergetisch de koudetolerantie van meloenen?
- Wat is het phylum van mitochondria?
- Hoe transporteert het celtransportwater over het membraan?
- Wetenschappers koppelen eicelspecifieke histon H1FOO aan een betere iPS-celgeneratie
- Optimalisatie van een nieuwe spuitmethode voor keramische coatings

- Betrouwbare detectie van bijsmaken van cacao

- Onderzoeksteam toont complexe, 3D-geprinte schwarzieten zijn bestand tegen druk wanneer ze zijn gecoat

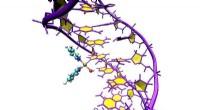
- Hoe interageren metalen met DNA?
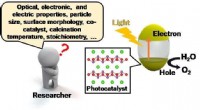
- De reis naar schone energie versnellen door optimalisatie van fotokatalysatoren
 Internationaal team visualiseert eigenschappen van celwanden van planten op nanoschaal
Internationaal team visualiseert eigenschappen van celwanden van planten op nanoschaal Californië lijkt een droge, warme winter
Californië lijkt een droge, warme winter Waarom worden we ziek?
Waarom worden we ziek?  Wat moet er gebeuren voordat een trechterwolk als tornado wordt geclassificeerd?
Wat moet er gebeuren voordat een trechterwolk als tornado wordt geclassificeerd?  Wat zijn kenmerken van Arachnida?
Wat zijn kenmerken van Arachnida?  Wat is de vrijetijdsbosstatus?
Wat is de vrijetijdsbosstatus?  Een over het hoofd gezien stukje van de zonnedynamo-puzzel
Een over het hoofd gezien stukje van de zonnedynamo-puzzel Video:Gaia astronomische revolutie
Video:Gaia astronomische revolutie
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

