
Wetenschap
Een molecuul met tegengestelde ladingen op uiteinden?
Dit is waarom:
* polariteit: Een molecuul is polair wanneer het ene uiteinde een enigszins positieve lading heeft (Δ+) en het andere uiteinde een enigszins negatieve lading heeft (Δ-). Dit ladingsverschil is te wijten aan een ongelijke verdeling van elektronen.
* elektronegativiteit: De ongelijke verdeling van elektronen komt voort uit het verschil in elektronegativiteit tussen de atomen in het molecuul. Elektronegativiteit is het vermogen van een atoom om elektronen naar zichzelf aan te trekken in een binding.
* Atomen met hogere elektronegativiteit trekken elektronen sterker aan, waardoor een gedeeltelijke negatieve lading (A-) om hen heen ontstaat.
* Atomen met lagere elektronegativiteit hebben een gedeeltelijke positieve lading (δ+).
Voorbeelden van polaire moleculen:
* water (h₂o): Zuurstof is elektronegatiefer dan waterstof, wat resulteert in een negatieve lading op het zuurstofatoom en een positieve lading op de waterstofatomen.
* waterstofchloride (HCl): Chloor is elektronegatiefer dan waterstof, waardoor een negatieve lading op het chlooratoom en een positieve lading op het waterstofatoom ontstaat.
* koolstofdioxide (co₂): Hoewel elk zuurstofatoom een negatieve lading heeft, is het molecuul lineair en symmetrisch. Dit betekent dat de kosten worden opgeheven, waardoor het molecuul algemeen niet -polair wordt.
Laat het me weten als je meer details wilt over poolmoleculen of nog andere vragen hebt!
 Terug naar het wild:hoe ‘ungardening’ wortel schoot in Amerika
Terug naar het wild:hoe ‘ungardening’ wortel schoot in Amerika  De meeste van de laatste 11, 000 jaar koeler dan het afgelopen decennium in Noord-Amerika, Europa
De meeste van de laatste 11, 000 jaar koeler dan het afgelopen decennium in Noord-Amerika, Europa Verontwaardiging over wetsvoorstel in Brazilië om milieuregels te versoepelen
Verontwaardiging over wetsvoorstel in Brazilië om milieuregels te versoepelen Te dichtbij of te ver? Wat fruitvliegjes ons leren over persoonlijke ruimte
Te dichtbij of te ver? Wat fruitvliegjes ons leren over persoonlijke ruimte  Voorspelling orkaan in de Stille Oceaan gecompliceerd door coronavirus
Voorspelling orkaan in de Stille Oceaan gecompliceerd door coronavirus
Hoofdlijnen
- Waaruit bestaat het menselijk hart? Onderzoekers analyseren cijfers
- Waarom oudere vaders meer genetische mutaties doorgeven aan hun nakomelingen
- Waarom zijn sommige mensen muggenmagneten en anderen niet? Entomoloog wijst op stofwisseling, lichaamsgeur en mindset
- Hoe werkt DNA-vertaling?
- Beschrijf het weefseltype en de functie van een pees?
- De adelaars scouten:het bewijs dat het beschermen van nesten de voortplanting bevordert
- Schubben of veren? Het komt allemaal neer op een paar genen
- Wat doen de rhizoïden van bryophytes?
- De voor- en nadelen van klonen
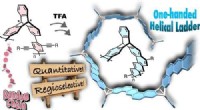
- Synthese van spiraalvormige ladderpolymeren
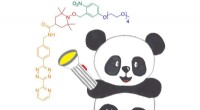
- Een nieuwe eiwit-spin-labelingtechniek
- Onderzoekers realiseren de ideale elektronische structuur van kagome-metaal

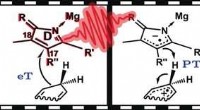
- Stapsgewijze hydrideoverdracht in de biosynthese van chlorofyl
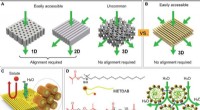
- Zelf-geassembleerd membraan met water-continue transportroutes voor nauwkeurige nanofiltratie
 Is het veilig om de dampen in te ademen van verwarmde koperdraad?
Is het veilig om de dampen in te ademen van verwarmde koperdraad?  Betekent een HR -diagram de helderheid van een sterren en oppervlaktetemperatuur?
Betekent een HR -diagram de helderheid van een sterren en oppervlaktetemperatuur?  Is het waar dat enzymen het aantal botsingen in een chemische reactie verhogen?
Is het waar dat enzymen het aantal botsingen in een chemische reactie verhogen?  Het moiré-effect gebruiken om transparante afbeeldingen te maken
Het moiré-effect gebruiken om transparante afbeeldingen te maken Waarom vast natriumchloride geleiden?
Waarom vast natriumchloride geleiden?  Wat is de naam van het eerste ruimtevaartuig tot de ruimte?
Wat is de naam van het eerste ruimtevaartuig tot de ruimte?  Nieuw onderzoek laat zien hoe onderzees grondwater de groei van koraalriffen beïnvloedt
Nieuw onderzoek laat zien hoe onderzees grondwater de groei van koraalriffen beïnvloedt Bevooroordeelde wervingspraktijken, inflexibele schema's benadelen moeders op de hele arbeidsmarkt
Bevooroordeelde wervingspraktijken, inflexibele schema's benadelen moeders op de hele arbeidsmarkt
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

