
Wetenschap
Hoe is de chemische formule voor een zuur dat verschilt van een basis?
zuren:
* Algemene formule: Begin meestal met h (waterstof), gevolgd door een niet-metaal of een polyatomisch ion.
* in oplossing: Ze geven waterstofionen vrij (H+) Wanneer opgelost in water, waardoor de oplossing zuurder wordt.
* Voorbeelden: HCl (zoutzuur), HNO3 (salpeterzuur), H2SO4 (zwavelzuur), CH3COOH (azijnzuur)
Bases:
* Algemene formule: Bevatten meestal A metal of ammoniak (NH3) .
* in oplossing: Ze geven hydroxide-ionen vrij (oh-) Wanneer opgelost in water, waardoor de oplossing meer alkalisch is (Basic).
* Voorbeelden: NaOH (natriumhydroxide), KOH (kaliumhydroxide), Ca (OH) 2 (calciumhydroxide), NH3 (ammoniak)
belangrijke opmerkingen:
* Niet alle verbindingen die beginnen met h zijn zuren: H2O (water) is bijvoorbeeld neutraal.
* Niet alle verbindingen die OH bevatten, zijn bases: CH3OH (methanol) is bijvoorbeeld geen basis.
* Er zijn ook Brønsted-Lowry en Lewis zuur-base theorieën: Deze theorieën richten zich op het vermogen om respectievelijk protonen of elektronenparen te doneren of te accepteren, die de definitie kunnen uitbreiden die verder gaat dan alleen H+ en OH-.
Samenvattend, hoewel de algemene formule een nuttige indicator kan zijn, is de het definiëren van kenmerk van zuren de afgifte van H+ -ionen, terwijl basen oh-ionen vrijgeven wanneer opgelost in water.
 Wat hebben mechanische chemische elektrische software en civiel gemeen?
Wat hebben mechanische chemische elektrische software en civiel gemeen?  Wat is een voorbeeld van een amorfe vaste stof?
Wat is een voorbeeld van een amorfe vaste stof?  Wat is een ander woord dat wordt gebruikt om een waterstofion te beschrijven?
Wat is een ander woord dat wordt gebruikt om een waterstofion te beschrijven?  Geef het belangrijkste type opgeloste interactie en rangoplossingen van de zwakste tot sterkste KCL in water CH2CL2 benzeen C6H6 CH3OH H2O?
Geef het belangrijkste type opgeloste interactie en rangoplossingen van de zwakste tot sterkste KCL in water CH2CL2 benzeen C6H6 CH3OH H2O?  Overgangsmetaalcomplexen:gemengd werkt beter
Overgangsmetaalcomplexen:gemengd werkt beter
 Wat als je vriend een plan heeft, een experiment voor wetenschapsbeurs, hij vraagt hulp dat zijn onderwerp de sterkste stoffen rugzakken is wat variabelen moeten opnemen?
Wat als je vriend een plan heeft, een experiment voor wetenschapsbeurs, hij vraagt hulp dat zijn onderwerp de sterkste stoffen rugzakken is wat variabelen moeten opnemen?  Hoe vormt water aardse landschappen?
Hoe vormt water aardse landschappen?  Schatten van de kustwaterdiepte vanuit de ruimte via satellietgebaseerde bathymetrie
Schatten van de kustwaterdiepte vanuit de ruimte via satellietgebaseerde bathymetrie  Onvermoeibare ecosysteemingenieurs of hinderlijke dieren? De aanwezigheid van bevers was voelbaar in de Boise River
Onvermoeibare ecosysteemingenieurs of hinderlijke dieren? De aanwezigheid van bevers was voelbaar in de Boise River  Het boek van de professor schetst hoe gemeenschappen het onderwijs kunnen hervormen
Het boek van de professor schetst hoe gemeenschappen het onderwijs kunnen hervormen
Hoofdlijnen
- Federale overheid:geen lijst van bedreigde soorten voor walrus
- Wat zijn enkele moleculen die bewegen door diffusie en osmose?
- Welke twee paringsbacteriën AME cel-tot-celcontact door een dunne tijdelijke cytoplasmatische brug waardoor het plasmide van cel naar andere cel reist?
- Hoe klimaatverandering de overdracht van malaria zal beïnvloeden
- Waar komt genectische variatie vandaan?
- Zal deze cel langer worden tijdens de mitose?
- Hoe kan de evolutie van een kenmerk binnen de ene soort een andere soort beïnvloeden?
- Welke cellaag ontwikkelen laterale wortels?
- Welke dieren kunnen het coronavirus oplopen?
- Analyse van biologische en chemische schade aan 20e-eeuwse bouwmaterialen

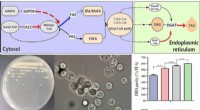
- Celfabriek die zeer zuiver DHA kan produceren
- Superresolutiemicroscopie:nog dichter bij de limiet komen

- Nieuwe techniek maakt snelle screening op nieuwe typen zonnecellen mogelijk

- Nieuw hulpmiddel voor de kristallisatie van eiwitten
 Mysterie van hoe sperma zwemt onthuld in wiskundige formule
Mysterie van hoe sperma zwemt onthuld in wiskundige formule Waarom zullen sommige stoffen in de chromatografie verder op het papier terechtkomen?
Waarom zullen sommige stoffen in de chromatografie verder op het papier terechtkomen?  IJzig Europa, zwoele Noordpool:de wereld op zijn kop
IJzig Europa, zwoele Noordpool:de wereld op zijn kop Is het oplossen van zout in wateromkeerbaar of onomkeerbaar?
Is het oplossen van zout in wateromkeerbaar of onomkeerbaar?  Op een dag, een vliegtuig kan je vlieglessen geven
Op een dag, een vliegtuig kan je vlieglessen geven Hoe helpen oceaangraven uit te leggen waarom korst toegevoegd bij richels de aarde groter maakt?
Hoe helpen oceaangraven uit te leggen waarom korst toegevoegd bij richels de aarde groter maakt?  Welke sedimentaire rots is gemaakt van grote hoekstukken sedimenten?
Welke sedimentaire rots is gemaakt van grote hoekstukken sedimenten?  Wetenschappers ontdekken de mysteries van hoe virussen evolueren
Wetenschappers ontdekken de mysteries van hoe virussen evolueren
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

