
Wetenschap
185 gram KOH en 1350 H2O Wat is molariteit?
1. Bereken de mol KOH
* Molaire massa van KOH: 39.10 g/mol (k) + 16,00 g/mol (o) + 1,01 g/mol (H) =56,11 g/mol
* mol KOH: (185 g KOH) / (56,11 g / mol) =3,30 mol KOH
2. Bereken het volume van de oplossing
* Dichtheid van water: Neem aan dat de dichtheid van water 1 g/ml is.
* watervolume: (1350 g h₂o) / (1 g / ml) =1350 ml
* Totaal volume van oplossing: Omdat het volume KOH te verwaarlozen is in vergelijking met het water, kunnen we het totale volume als 1350 ml benaderen.
3. Converteer volume naar liters
* Volume in liters: 1350 ml / 1000 ml / l =1,35 l
4. Molariteit berekenen
* molariteit (m): (3.30 mol KOH) / (1,35 l) = 2,44 m
Daarom is de molariteit van de KOH -oplossing ongeveer 2,44 m.
 VS handhaaft luchtvervuilingsnorm onder Obama
VS handhaaft luchtvervuilingsnorm onder Obama Smog dwingt inwoners van Peking om te innoveren voor de wereld
Smog dwingt inwoners van Peking om te innoveren voor de wereld Stijgende temperaturen bedreigen de stabiliteit van de Tibetaanse alpengraslanden
Stijgende temperaturen bedreigen de stabiliteit van de Tibetaanse alpengraslanden Hoe een verbeterde groene infrastructuur in de binnenstad de volksgezondheid kan verbeteren
Hoe een verbeterde groene infrastructuur in de binnenstad de volksgezondheid kan verbeteren Soorten schimmels Planten
Soorten schimmels Planten
Hoofdlijnen
- Wat zijn de eenvoudigste vormen van materie die kunnen bestaan onder normale laboratoriumomstandigheden?
- Hoeveel paar chromosomen zijn er in een menselijke huidcelproductie door mitose?
- Bloemstroken en heggen geven samen een boost aan bijen in boomgaarden
- Wat is de oorzaak van een tekort aan zowel rode als witte bloedcellen?
- Is een blaarkever een omnivoor?
- Stijgende zeetemperaturen bedreigen Atlantische populaties van Bulwers-stormvogels
- Hoe is de breedste categorie in de biologische taxonomie?
- Onderzoekers ontdekken menselijk DNA-herstel door middel van nucleaire metamorfose
- Hoe de ziekteverwekker Mycobacterium tuberculosis zijn enige bekende exotoxine uitscheidt en distribueert
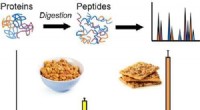
- Catcher van de roggemethode detecteert roggegluteneiwitten in voedingsmiddelen
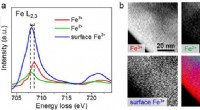
- Efficiënte waterstofconversie door splitsing van water door zonne-energie met behulp van op hematiet-mesocrystal gebaseerde fotoanodes
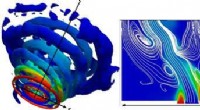
- Minimalisering van de uitstoot van ammoniakbrandstof
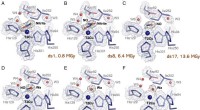
- Moleculaire films werpen licht op het enzym dat betrokken is bij de productie van broeikasgassen
- Aaí bessenextracten bestrijden malaria bij muizen
 Blijven of vertrekken? Een verhaal over twee virusstrategieën onthuld door wiskunde
Blijven of vertrekken? Een verhaal over twee virusstrategieën onthuld door wiskunde  Hoe Punnett Squares
Hoe Punnett Squares Is een glazen microscoopschuifgeleider of isolator?
Is een glazen microscoopschuifgeleider of isolator?  Een duidelijk zicht door mist van stadstoezicht
Een duidelijk zicht door mist van stadstoezicht Waarom moeten cellen sterven?
Waarom moeten cellen sterven?  Welk eilandlocatie is 15 graden oost en 38 North?
Welk eilandlocatie is 15 graden oost en 38 North?  Essay:Zal het Eerste Amendement het informatietijdperk overleven?
Essay:Zal het Eerste Amendement het informatietijdperk overleven?  Game on Mom and Dad:onderzoekers roepen ouders op om hun gebruik van videogames te bespreken
Game on Mom and Dad:onderzoekers roepen ouders op om hun gebruik van videogames te bespreken
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

