
Wetenschap
De molaire oplosbaarheid van wordt niet beïnvloed door de pH -oplossing NA3PO4 NAF KNO3 ALCL3 of MNS?
Molaire oplosbaarheid en pH begrijpen
* Molaire oplosbaarheid: De molaire oplosbaarheid van een zout is de concentratie van het metaalkation (of anion) in een verzadigde oplossing bij een gegeven temperatuur.
* pH: PH meet de zuurgraad of basiciteit van een oplossing.
Hoe pH de oplosbaarheid beïnvloedt
De pH van een oplossing kan de oplosbaarheid van zouten beïnvloeden die zwakke zuren of basen omvatten. Dit komt omdat het evenwicht van de oplosreactie kan worden verschoven door de aanwezigheid van H+ of OH-ionen.
Analyse van de zouten
Laten we elk zout onderzoeken:
* Na3po4 (natriumfosfaat): Fosfaationen (PO43-) zijn de conjugaatbasis van een zwak zuur (H3PO4). In zure oplossingen zullen H+ -ionen reageren met PO43- om H3PO4 te vormen, waardoor het oplossing-evenwicht naar rechts wordt verplaatst, waardoor de oplosbaarheid toeneemt. In basisoplossingen zullen OH-ionen een minimaal effect hebben op de oplosbaarheid.
* NAF (natriumfluoride): Fluoride-ionen (F-) zijn de conjugaatbasis van een zwak zuur (HF). Net als fosfaat zal de oplosbaarheid van NAF toenemen in zure oplossingen als gevolg van de reactie van H+ met F-.
* KNO3 (kaliumnitraat): Nitraationen (NO3-) zijn de conjugaatbasis van een sterk zuur (HNO3). Sterke zuren/basen hebben geen invloed op de oplosbaarheid van hun geconjugeerde basen, dus de pH heeft geen invloed op de oplosbaarheid van KNO3.
* alcl3 (aluminium chloride): Aluminiumchloride omvat geen zwak zuur of basis. De pH zal zijn oplosbaarheid niet significant beïnvloeden.
* mns (mangaan (ii) sulfide): Sulfide-ionen (S2-) zijn de conjugaatbasis van een zwak zuur (H2S). De oplosbaarheid van MNS zal toenemen in zure oplossingen vanwege de reactie van H+ met S2-.
Conclusie
De zouten waarvan de oplosbaarheid van de mol wordt beïnvloed door de pH van de oplossing, zijn:
* Na3po4 (natriumfosfaat)
* NAF (natriumfluoride)
* mns (mangaan (ii) sulfide)
Belangrijke opmerking: De oplosbaarheid van deze zouten zal toenemen in zure oplossingen en afname van basisoplossingen.
 Kristallijne kunstmatige spier zorgt ervoor dat papieren pop sit-ups doet
Kristallijne kunstmatige spier zorgt ervoor dat papieren pop sit-ups doet Wat zijn de 6 elementen van de wetenschappelijke methode?
Wat zijn de 6 elementen van de wetenschappelijke methode?  Katalysatorvooruitgang kan leiden tot zuinige brandstofcellen
Katalysatorvooruitgang kan leiden tot zuinige brandstofcellen Waarom zijn ionische verbindingen niet oplosbaar in niet-waterige oplossingen zoals benzine?
Waarom zijn ionische verbindingen niet oplosbaar in niet-waterige oplossingen zoals benzine?  Welke kleur geeft groen en rood gemengd?
Welke kleur geeft groen en rood gemengd?
 Eerdere snelle opwarmingsniveaus in het noordpoolgebied geassocieerd met wijdverbreide klimaatveranderingen
Eerdere snelle opwarmingsniveaus in het noordpoolgebied geassocieerd met wijdverbreide klimaatveranderingen Hoe vrienden te maken met een eekhoorn
Hoe vrienden te maken met een eekhoorn  Is een lommerige zeedragonplant of dier?
Is een lommerige zeedragonplant of dier?  Kan het eten van insectenpoeder en schimmelvlees helpen bij het bestrijden van klimaatverandering? Ja, maar er zijn eenvoudigere manieren
Kan het eten van insectenpoeder en schimmelvlees helpen bij het bestrijden van klimaatverandering? Ja, maar er zijn eenvoudigere manieren Kunnen milieuschendingen olie- en gasbedrijven definiëren als slechte actoren? Er wacht een oordeel
Kunnen milieuschendingen olie- en gasbedrijven definiëren als slechte actoren? Er wacht een oordeel
Hoofdlijnen
- Wat voor soort vragen kan wetenschap Anwser?
- Typen agarplaten
- Vertoont een levend organisme alle levensduur van de kenmerken?
- Emotie kan ervoor zorgen dat kippen rood in het gezicht krijgen
- Waar denken sommige wetenschappers dat de eenvoudige bacteriën die ooit alleen de vorm van leven op aarde waren, ontstonden?
- Wat is een beschrijvingscellen?
- Wat is een spoel van mitochondria?
- Fermentatie treedt op wanneer een cel wordt?
- Hoe verhouden de processen van fotosynthese en cellulaire ademhaling tot elkaar?
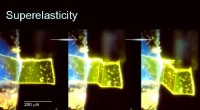
- Rood licht voor stress:een van kleur veranderend organisch kristal
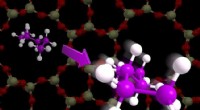
- Onderzoekers ontdekken hoe moleculen in kooien ratelen en zingen
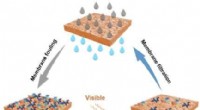
- Wetenschappers ontwikkelen N-gedoteerde zelfreinigende membranen die gebruik maken van bestraling met zichtbaar licht
- Moleculair viroloog bestrijdt griep op moleculair niveau

- Elementen in planten gebruiken om de efficiëntie van de brandstofcel te verhogen en tegelijkertijd de kosten te verlagen

 Waarom is de zonnestraling sterker op het zuidelijk halfrond?
Waarom is de zonnestraling sterker op het zuidelijk halfrond?  De Super-Kamiokande-detector wacht op neutrino's van een supernova
De Super-Kamiokande-detector wacht op neutrino's van een supernova Wat is de helft van nul graden Celsius?
Wat is de helft van nul graden Celsius?  Onderzoekers maken beelden met hoge resolutie van magnesiumionen die interageren met het genbewerkingsenzym CRISPR
Onderzoekers maken beelden met hoge resolutie van magnesiumionen die interageren met het genbewerkingsenzym CRISPR  Nepalese klimmers overwonnen verraderlijke omstandigheden om geschiedenis te schrijven op K2
Nepalese klimmers overwonnen verraderlijke omstandigheden om geschiedenis te schrijven op K2 Hoeveel bewoonbare planeten zijn er?
Hoeveel bewoonbare planeten zijn er? Kunstmatige intelligentie verslaat ons bij het schaken, maar niet in het geheugen
Kunstmatige intelligentie verslaat ons bij het schaken, maar niet in het geheugen Wat is de belangrijkste energiebron die je aarde verwarmt?
Wat is de belangrijkste energiebron die je aarde verwarmt?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

