
Wetenschap
Welke soorten metaal zijn gesuscepitibel voor corrosie?
metalen zeer gevoelig voor corrosie:
* ijzer en staal: Dit zijn de meest voorkomende en ook een van de meest gemakkelijk gecorrodeerde. IJzer roest in aanwezigheid van zuurstof en water.
* roestvrij staal: Hoewel beter bestand, kunnen bepaalde soorten roestvrij staal nog steeds corroderen, vooral in harde omgevingen of als de beschermende oxidelaag wordt beschadigd.
* aluminium: Aluminium vormt een beschermende oxidelaag die typisch verdere corrosie voorkomt. Deze laag kan echter worden aangetast in zure of alkalische omgevingen, wat leidt tot putjes of galvanische corrosie.
* koper en zijn legeringen (messing, brons): Deze metalen zijn relatief corrosiebestendig, maar ze kunnen gevoelig zijn voor aangetaste en groene patina-vorming (koperoxiden) in vochtige of vervuilde omgevingen.
* magnesium: Magnesium is relatief licht en sterk, maar het corrodeert snel in vochtige lucht of water.
* zink: Gebruikt voor galvanisatie (coatingstaal om roest te voorkomen), zink is corrosiebestendig maar kan corroderen in specifieke omgevingen.
Factoren die de corrosie beïnvloeden:
* omgeving: Vocht, vochtigheid, zoutgehalte, zuurgraad en de aanwezigheid van verontreinigende stoffen spelen allemaal een belangrijke rol in hoe snel een metaal corrodeert.
* Temperatuur: Hogere temperaturen versnellen meestal corrosiesnelheden.
* Stress: Mechanische stress op een metaal kan gebieden creëren waar de beschermende oxidelaag dunner is, waardoor deze gevoeliger is voor corrosie.
* metalen samenstelling: De aanwezigheid van onzuiverheden of legeringselementen kan de gevoeligheid van een metaal voor corrosie veranderen.
* Elektrochemische interacties: Wanneer twee ongelijksoortige metalen in contact zijn in een elektrolyt (zoals zoutwater), kan corrosie optreden als gevolg van galvanische werking.
Voorbeelden van corrosietypen:
* roesten: De vorming van ijzeroxide (roest) op ijzer of staal.
* putjes: Gelokaliseerde corrosie die gaten of kuilen in het metalen oppervlak creëert.
* Galvanische corrosie: Treedt op wanneer twee ongelijksoortige metalen in contact staan in een elektrolyt, waardoor het ene metaal sneller wordt gecorrodeerd dan het andere.
* Stresscorrosie kraken: Een type corrosie dat optreedt onder stress en in specifieke omgevingen.
Corrosie voorkomen:
* coatings: Verf, vernis of andere beschermende coatings kunnen werken als een barrière tussen het metaal en de omgeving.
* Galvanisatie: Het aanbrengen van een zinkcoating op een metaal, zoals staal, kan corrosie voorkomen.
* legering: Het toevoegen van andere metalen aan een legering kan zijn weerstand tegen corrosie verbeteren.
* Kathodische bescherming: Een externe bron van elektrische stroom gebruiken om corrosie te voorkomen.
Vergeet niet dat corrosie een complex proces is en de gevoeligheid ervan varieert, afhankelijk van het specifieke metaal, de omgeving en andere factoren.
 Waarom bezorgen bepaalde ervaringen ons kippenvel?
Waarom bezorgen bepaalde ervaringen ons kippenvel?  Bleken treft 's werelds zuidelijkste koraalrif:wetenschappers
Bleken treft 's werelds zuidelijkste koraalrif:wetenschappers Interne waakhond zegt dat EPA het opruimen van giftige sites verkeerd beheert
Interne waakhond zegt dat EPA het opruimen van giftige sites verkeerd beheert Een droger zuiden:de droogtetrends in Europa komen overeen met de prognoses van klimaatverandering
Een droger zuiden:de droogtetrends in Europa komen overeen met de prognoses van klimaatverandering Een nieuwe draai aan het verhaal over de oorsprong van uranium, door CSU-wetenschappers
Een nieuwe draai aan het verhaal over de oorsprong van uranium, door CSU-wetenschappers
Hoofdlijnen
- Wat is het principe van parsimony in de biologie?
- Wat is uitscheiding in de wetenschap?
- Zijn erraden en mitochondriën twee gespecialiseerde cellen alleen in planten gevonden?
- Wat zijn de eiwitten ingebed in lipide dubbellaag?
- Wanneer enzymen worden geplaatst in extreme pH- of temperatuuromstandigheden, ontspannen ze en veranderen van vorm, wat wordt dit genoemd?
- Wat dient als de kern voor amoebas en protozoën?
- Nieuwe studie heeft tot doel de redenen te begrijpen waarom genitale snijden bij vrouwen aanhoudt (update)
- Wat experimenteerde Frederick met muizen?
- Onderzoekers tonen aan dat generalistische soorten ‘manusje-van-alles zijn en alles beheersen’
- De geheimen van Tennessee whisky ontrafelen

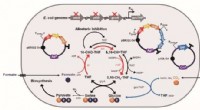
- Gemanipuleerde E. coli met mierenzuur en CO2 als een C1-raffinaderijplatformstam
- Wat maakt kobalt essentieel voor het leven?

- Slimme polymeren zetten elektrische energie om in mechanisch werk

- Enigma van vetzuurmetabolisme opgelost - enzymvorm regelt activiteit
 Onderzoek toont aan hoe elektriciteitetende microben elektronen gebruiken om koolstofdioxide vast te leggen
Onderzoek toont aan hoe elektriciteitetende microben elektronen gebruiken om koolstofdioxide vast te leggen  Team bevordert elektronische DNA-sequencing met één molecuul
Team bevordert elektronische DNA-sequencing met één molecuul Wiskundigen ontwikkelen nieuwe klassen van oplossingen voor stellaire dynamische systemen
Wiskundigen ontwikkelen nieuwe klassen van oplossingen voor stellaire dynamische systemen Natuurlijke landschappen? Wetenschappers roepen op tot een paradigmaverschuiving in restauratieprojecten
Natuurlijke landschappen? Wetenschappers roepen op tot een paradigmaverschuiving in restauratieprojecten  De verrassende omgeving van een raadselachtige neutronenster
De verrassende omgeving van een raadselachtige neutronenster Hoe komen de spermacellen in een stuifmeelkorrel aan bij de eicelklus in een plant-ovule?
Hoe komen de spermacellen in een stuifmeelkorrel aan bij de eicelklus in een plant-ovule?  Hoe te berekenen Percentage Error
Hoe te berekenen Percentage Error Waarom ontploft de telefoon?
Waarom ontploft de telefoon?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

