
Wetenschap
Welke massa NH3 wordt geproduceerd wanneer 1.20 mol N2 volledig reageert in de volgende vergelijking plus 3H2 2NH3?
1. Evenwichtige chemische vergelijking:
De evenwichtige chemische vergelijking voor de reactie is:
N₂ + 3H₂ → 2NH₃
2. Mol -verhouding:
Uit de evenwichtige vergelijking zien we dat 1 mol N₂ 2 mol NH₃ produceert.
3. Bereken mol NH₃:
Omdat we 1,20 mol N₂ hebben, kunnen we de molverhouding gebruiken om de mol NH₃ geproduceerd te vinden:
1.20 mol N₂ * (2 mol NH₃ / 1 mol N₂) =2,40 mol NH₃
4. Converteer mols naar massa:
Om mol NH₃ om te zetten in massa, gebruiken we de molaire massa van NH₃ (17,03 g/mol):
2.40 mol NH₃ * (17.03 g nH₃ / 1 mol nH₃) = 40,9 g nh₃
Daarom wordt 40,9 g NH₃ geproduceerd wanneer 1,20 mol N₂ volledig reageert.
 Robotachtige drijvers geven een nieuwe kijk op de gezondheid van de oceaan en de wereldwijde koolstofcyclus
Robotachtige drijvers geven een nieuwe kijk op de gezondheid van de oceaan en de wereldwijde koolstofcyclus Wat zijn de 8 ecosystemen?
Wat zijn de 8 ecosystemen?  Nieuw onderzoek naar Darwins vinken biedt een zeldzaam inzicht in hoe soorten uiteenlopen
Nieuw onderzoek naar Darwins vinken biedt een zeldzaam inzicht in hoe soorten uiteenlopen  Klimaatverandering bestrijden is enorm populair, maar de meeste Amerikanen weten dat niet
Klimaatverandering bestrijden is enorm populair, maar de meeste Amerikanen weten dat niet Meeuwen:schildwachten van bacteriën in de omgeving
Meeuwen:schildwachten van bacteriën in de omgeving
Hoofdlijnen
- Welk weefsel vertoont in overvloed chloroplasten?
- Wat is een kenmerk van een hypothese?
- Welke cel heeft een of meer grote vacuolen?
- Bootverkeer bedreigt het voortbestaan van de Bocas Del Toro-dolfijnen in Panama
- Wetenschappers ontrafelen mysteries van DNA-replicatie in maïs
- Waarom begon Mendel zijn experimenten door eren te laten pollineren voor meerdere generaties?
- Studie onthult hoe DNA zich ontvouwt voor transcriptie
- Wat is de functie van het zenuwstelsel?
- Nu Rusland Oekraïne binnenvalt, wat is op dit moment de dreiging van een nucleaire oorlog?
- Dat nieuwe garen?! - Draagbaar, wasbare textielapparaten zijn mogelijk met MXene-gecoate garens

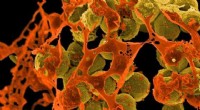
- Wetenschappers maken belangrijke doorbraak op weg naar nieuw superbug-dodend antibioticum teixobactine
- Op zoek naar een behandeling voor IBS-pijn in tarantulagif

- Een Rubiks microfluïdische kubus

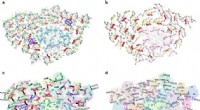
- Structuur van supercomplex van fotosysteemproteïne van diatomeeën onthult zijn zeer geavanceerde energieoverdrachtsnetwerk
 Wetenschappers voeren HONO verticale gradiëntobservaties uit om nieuwe bevindingen te verkrijgen
Wetenschappers voeren HONO verticale gradiëntobservaties uit om nieuwe bevindingen te verkrijgen Hoe is het om een orkaan van categorie 5 te ervaren?
Hoe is het om een orkaan van categorie 5 te ervaren?  Welke stoffen is een reactant in fotosynthese?
Welke stoffen is een reactant in fotosynthese?  Waarom kunnen flexibiliteit en ruimdenkende wenselijke kwaliteiten zijn bij een wetenschapper?
Waarom kunnen flexibiliteit en ruimdenkende wenselijke kwaliteiten zijn bij een wetenschapper?  Wat veroorzaken onevenwichtige krachten een object?
Wat veroorzaken onevenwichtige krachten een object?  Wat zijn voorbeelden van fysische chemische en nucleaire verandering in dezelfde kwestie?
Wat zijn voorbeelden van fysische chemische en nucleaire verandering in dezelfde kwestie?  Regels voor het vermenigvuldigen van wetenschappelijke notatie
Regels voor het vermenigvuldigen van wetenschappelijke notatie Gaia ziet twee tijdelijk vergrote sterren
Gaia ziet twee tijdelijk vergrote sterren
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

