
Wetenschap
Wat is de naam van substantie met formule FE2O2?
Dit is waarom:
* De gemeenschappelijke oxidatie van ijzer staat: IJzer bestaat typisch in twee gemeenschappelijke oxidatietoestanden:+2 (ferro) en +3 (ferrisch).
* oxidatietoestand van Oxygen: Zuurstof heeft bijna altijd een oxidatietoestand van -2.
* Balancingskosten: Om de ladingen in een verbinding in evenwicht te brengen, moet de som van de oxidatietoestanden van alle atomen gelijk zijn aan nul.
* fe₂o₂: In deze formule zou de oxidatietoestand van ijzer +1 moeten zijn om de -4 -lading van de twee zuurstofatomen in evenwicht te brengen. IJzer bestaat echter zelden in een +1 oxidatietoestand.
Daarom is Fe₂o₂ geen bekende stabiele verbinding.
Mogelijke verkeerde interpretaties:
* Feo: Dit is de formule voor ijzer (ii) oxide , ook bekend als ferro -oxide.
* fe₂o₃: Dit is de formule voor ijzer (iii) oxide , ook bekend als ijzeroxide of roest .
Het is belangrijk om de chemische formule te controleren en ervoor te zorgen dat deze een geldige en stabiele verbinding vertegenwoordigt.
 Kun je een doel geven voor het bakken van frisdrank vulkaan?
Kun je een doel geven voor het bakken van frisdrank vulkaan?  Hoe beïnvloedt de temperatuur de oplosbaarheid van de meeste vaste stoffen?
Hoe beïnvloedt de temperatuur de oplosbaarheid van de meeste vaste stoffen?  Is wolk een vaste vloeistof of gas?
Is wolk een vaste vloeistof of gas?  Chemici ontwikkelen een raamwerk om een efficiënte synthese van informatierijke moleculen mogelijk te maken
Chemici ontwikkelen een raamwerk om een efficiënte synthese van informatierijke moleculen mogelijk te maken Welk homogeen mengsel ontstaat wanneer suiker wordt opgelost in een glas heet water?
Welk homogeen mengsel ontstaat wanneer suiker wordt opgelost in een glas heet water?
 Vraag en antwoord:impact van inspanningen om ontbossing in Amazone te verminderen overschat, studie vondsten
Vraag en antwoord:impact van inspanningen om ontbossing in Amazone te verminderen overschat, studie vondsten Stof droogt wolken op door waterdamp op te slokken:Wetenschappers laten zien hoe verschillende wolkenzaden het broeikaseffect kunnen beïnvloeden
Stof droogt wolken op door waterdamp op te slokken:Wetenschappers laten zien hoe verschillende wolkenzaden het broeikaseffect kunnen beïnvloeden  Bomen die snel leven sterven jong
Bomen die snel leven sterven jong Is worteltransplantatie een positief, coöperatief gedrag bij bomen?
Is worteltransplantatie een positief, coöperatief gedrag bij bomen?  Hoe noem je iets dat twee objecten in de buurt kan onderscheiden?
Hoe noem je iets dat twee objecten in de buurt kan onderscheiden?
Hoofdlijnen
- Uit onderzoek blijkt niet dat honden of wolven de reputatie van een mens kunnen begrijpen
- Geef de biologische betekenis van celademhaling?
- Wie zijn de Nebateeërs?
- Hoe verschilt een zegel van ijsbeer?
- Onderzoekers brengen het menselijk genoom in 4-D in kaart terwijl het vouwt
- Waarom sommige vissen 'junk' zijn en andere beschermd. Onderzoek wijst op vooroordelen tegen inheemse soorten
- Welk enzym is verantwoordelijk voor aerobe ademhaling?
- Wat is de naam van Square die wordt gebruikt om het fenotype van de genetische kruisende ouders te illustreren?
- Inheemse vissoorten lopen gevaar na verwijdering van water uit de Colorado-rivier
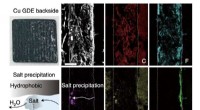
- Bifunctionele ionomeren gebruiken als elektrolyten om ethyleen uit koolstofdioxide te synthetiseren
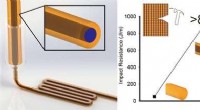
- Nieuwe techniek maakt snelle en goedkope productie van hoogwaardige circuits mogelijk

- 3D-printen van plastic onderdelen verbeteren
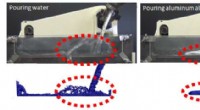
- Onderzoekers bootsen het gietgedrag van gesmolten metaal na met nieuw ontwikkelde simulatietechnologie
- Vloeibare kernvezels:er loopt een datarivier doorheen

 Studie onthult geheim leven van lithium in zonachtige sterren
Studie onthult geheim leven van lithium in zonachtige sterren Koolstofstippen van mensenhaar stimuleren zonnecellen
Koolstofstippen van mensenhaar stimuleren zonnecellen JRC-analyse helpt reactie op instorting van de dam in Laos
JRC-analyse helpt reactie op instorting van de dam in Laos Grafeen quantum dots:The next big small thing
Grafeen quantum dots:The next big small thing Pittige Tomaten,
Pittige Tomaten,  Wat is de hoofdkopie van een genetische code van een organismen?
Wat is de hoofdkopie van een genetische code van een organismen?  Studie helpt bij het begrijpen van onzichtbare maar machtige deeltjes
Studie helpt bij het begrijpen van onzichtbare maar machtige deeltjes Hoe kunnen alkalis vet en olie verwijderen?
Hoe kunnen alkalis vet en olie verwijderen?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

