
Wetenschap
Zal een metaalcorrode wanneer achtergelaten worden blootgesteld aan de omgeving en wordt aangevallen door niet -metaal chemische stof?
* Corrosie is een chemische reactie: Corrosie is een chemisch proces waarbij een metaal reageert met zijn omgeving, wat leidt tot de vorming van ongewenste verbindingen op het oppervlak. Dit kan het metaal verzwakken en ervoor zorgen dat het verslechtert.
* Niet -metalen chemicaliën kunnen corrosief zijn: Veel niet -metalen chemicaliën zijn zeer reactief met metalen. Voorbeelden zijn:
* zuren: Zuren zoals zoutzuur (HCL) en zwavelzuur (H₂so₄) vallen gemakkelijk metalen aan, vormen zouten en het vrijgeven van waterstofgas.
* zuurstof: Zuurstof in de lucht kan reageren met metalen in aanwezigheid van vocht, waardoor oxiden worden gevormd. Dit is een veel voorkomende vorm van corrosie die bekend staat als roest (voor ijzer).
* halogenen: Halogenen zoals chloor (CL₂) kunnen ook reageren met metalen om metaalhalogeniden te vormen.
* Omgevingsfactoren: De snelheid van corrosie kan worden beïnvloed door factoren zoals:
* vocht: Water werkt als een elektrolyt en versnelt het corrosieproces.
* Temperatuur: Hogere temperaturen verhogen in het algemeen de snelheid van corrosiereacties.
* aanwezigheid van zouten: Zouten kunnen de geleidbaarheid van water vergroten, waardoor het corrosiever wordt.
Voorbeelden:
* IJzer Rusting: IJzer reageert met zuurstof en water om ijzeroxide (roest) te vormen. Dit is een veel voorkomend voorbeeld van corrosie veroorzaakt door een niet -metalen chemische (zuurstof) in aanwezigheid van vocht.
* koper tarnishing: Koper reageert met zwavelverbindingen in de lucht om een groenachtige laag kopersulfide te vormen, bekend als trek. Dit is een ander voorbeeld van corrosie veroorzaakt door niet -metalen chemicaliën.
* aluminium reageert met zuren: Aluminium is een reactief metaal dat kan worden gecorrodeerd door zuren zoals zoutzuur, wat aluminiumchloride en waterstofgas produceert.
Samenvattend: Corrosie is een complex proces dat kan worden veroorzaakt door verschillende factoren, waaronder niet -metalen chemicaliën. De snelheid en het type corrosie zijn afhankelijk van het betrokken metaal, de specifieke chemische aanvallen die het aanvalt en omgevingscondities.
 Europeanen alert terwijl hittegolf intensiveert (update)
Europeanen alert terwijl hittegolf intensiveert (update) Hoe veranderen orkanen in landvormen?
Hoe veranderen orkanen in landvormen?  Natuurlijke blootstelling aan bosbrandrook verhoogde zwangerschapsverlies bij resusapen
Natuurlijke blootstelling aan bosbrandrook verhoogde zwangerschapsverlies bij resusapen Bosranden zijn mogelijk beter bestand tegen klimaatverandering dan eerder werd gedacht
Bosranden zijn mogelijk beter bestand tegen klimaatverandering dan eerder werd gedacht De delicate waterlelie:een roos met een andere naam?
De delicate waterlelie:een roos met een andere naam?
Hoofdlijnen
- Wat zijn de soorten bewustzijn?
- Wat zijn de fysieke eigenschappen van proteasen?
- Wat is een voorbeeld van niet -materie die wetenschapper bestudeert?
- Wat betekent bacteriën?
- Bij het vormen van nieuwe DNA -moleculen elke streng van uw handeling als een?
- Waar bevindt DNA zich in een multicellulair organisme?
- Een kenmerk van het spijsverteringsepitheel dat het expansieorgaan ondersteunt, is de aanwezigheid van?
- Antibioticaresistentie:onderzoekers slagen erin resistentiegenen te blokkeren
- Wat zijn de componenten van nucleotiden?
- Onderzoekers bepalen activeringsmechanisme van G-eiwit-gekoppelde receptoren

- Onderzoekers lossen eiwitstructuur op die verband houdt met erfelijke netvliesaandoeningen
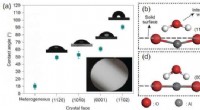
- Saffieren tonen hun ware kleuren:niet waterminnend
- Wetenschappers beschrijven de structuur van een toekomstige luminescentiestof

- Nieuw staal om de levensduur van olieveldpijpleidingen te verdubbelen

 Als er vorig leven op Mars bestond, het evolueerde samen met de omgeving van Mars
Als er vorig leven op Mars bestond, het evolueerde samen met de omgeving van Mars Bitterreceptor betrokken bij ontstekingsremmend effect van resveratrol?
Bitterreceptor betrokken bij ontstekingsremmend effect van resveratrol? Gedragsaanpassingen voor Sharks
Gedragsaanpassingen voor Sharks Bevat een skeletspiervezel veel kernen?
Bevat een skeletspiervezel veel kernen?  Drie manieren waarop blockchain de wereld ertoe kan brengen op te treden tegen de klimaatcrisis
Drie manieren waarop blockchain de wereld ertoe kan brengen op te treden tegen de klimaatcrisis Milieuvriendelijke veehouderij (echt waar)
Milieuvriendelijke veehouderij (echt waar) Gevormt koperoxide zich neer in water?
Gevormt koperoxide zich neer in water?  Hoeveel centimeter is gelijk aan 370 mm?
Hoeveel centimeter is gelijk aan 370 mm?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

