
Wetenschap
Wat is de pH van 0,02 m HCl?
Inzicht in de concepten
* HCl (zoutzuur): Een sterk zuur, wat betekent dat het volledig ioniseert in water.
* pH: Een maat voor de zuurgraad of alkaliteit van een oplossing. Hoe lager de pH, hoe zuurder de oplossing.
* pH -berekening: De pH van een oplossing wordt berekend met behulp van de volgende formule:
pH =-log [H+], waarbij [H+] de concentratie van waterstofionen is.
Berekening
1. Volledige ionisatie: Omdat HCl een sterk zuur is, ioniseert het volledig in water:
HCl (aq) → h + (aq) + cl- (aq)
Dit betekent dat een 0,02 M HCl -oplossing een concentratie van 0,02 M van H+ ionen zal produceren.
2. PH -berekening:
pH =-log [H+]
pH =-log (0,02)
pH ≈ 1.70
Daarom is de pH van een 0,02 M HCl -oplossing ongeveer 1,70.
 De zomers warmen sneller op dan de winters, zo blijkt uit fossiele schelpen uit Antwerpen
De zomers warmen sneller op dan de winters, zo blijkt uit fossiele schelpen uit Antwerpen  NASA ziet orkaan Jose voor de oostkust van de VS
NASA ziet orkaan Jose voor de oostkust van de VS Beving in Zuidwest-China laat 46 doden achter, veroorzaakt aardverschuivingen (update)
Beving in Zuidwest-China laat 46 doden achter, veroorzaakt aardverschuivingen (update) Duiken in de klimaatgeschiedenis van de Paaseilanden
Duiken in de klimaatgeschiedenis van de Paaseilanden Plasticvervuiling aanpakken:toptips van mariene wetenschappers
Plasticvervuiling aanpakken:toptips van mariene wetenschappers
Hoofdlijnen
- Wat is de combinatie van Darwiniaanse evolutietheorie en populatiegenetica die worden genoemd?
- Hoe verschilt gisting van cellulaire ademhaling?
- Wat is de lengte en breedte van de prokaryotische cel?
- Wat zijn catagorische gegevens?
- Welke informatie wordt overgedragen van de kern naar ribosoom geroepen?
- Waarom maken ecologen modellen?
- Hoe hebben de celorganismen overleefd als het zo klein is?
- Wat is erthrocyten?
- Bioreactorprocessen en cryotechnologieën verbeteren het testen van actieve ingrediënten met behulp van menselijke celculturen
- Ultraheldere röntgenstralen laten zien hoe planten binnen een fractie van een seconde op licht reageren

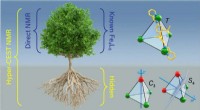
- Hyper-CEST NMR-techniek onthult ontbrekende structuur van een nieuw containermolecuul
- Thuis COVID-19-tests:hoe goed zijn ze?
- Eiwitvoeding voor cellen en organismen:kunnen we het gebruiken om ziekten te behandelen?
- Helderdere flexibele elektroluminescente film door de oogstructuur van nachtdieren aan te nemen

 Ethiopië opent fabriek om afval om te zetten in energie
Ethiopië opent fabriek om afval om te zetten in energie Wat is de opstelling van subatomaire deeltjes in 14C?
Wat is de opstelling van subatomaire deeltjes in 14C?  Wat zijn de functies van een magnetische magneetschakelaar?
Wat zijn de functies van een magnetische magneetschakelaar?  Welke kenmerken van het meest single celled organisme stellen hen in staat om hun levensactiviteiten voort te zetten en homeostase te behouden?
Welke kenmerken van het meest single celled organisme stellen hen in staat om hun levensactiviteiten voort te zetten en homeostase te behouden?  Hoe een oude steengroeve een wereldwijd geologisch referentiepunt werd
Hoe een oude steengroeve een wereldwijd geologisch referentiepunt werd Het einde van het tijdperk van fossiele brandstoffen?
Het einde van het tijdperk van fossiele brandstoffen?  Wetenschappers hebben methode uitgevonden om bacteriën te vangen met fotonische haak
Wetenschappers hebben methode uitgevonden om bacteriën te vangen met fotonische haak Wat zijn de mogelijke gevolgen van een mislukte supernova?
Wat zijn de mogelijke gevolgen van een mislukte supernova?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

